De surveillance van shigatoxineproducerende Escherichia coli (STEC (Shigatoxineproducerende E. coli-stammen)) in Nederland is in 1999 gestart met de meldingen van STEC O157-infecties. In 2007 zijn STEC non-O157-infecties hieraan toegevoegd, hoewel de surveillance op deze groep niet volledig landelijk dekkend is. Om mogelijke infectiebronnen vast te stellen onderzoekt de Nederlandse Voedsel- en Warenautoriteit (NVWA (Nederlandse Voedsel- en Warenautoriteit)) monsters van voeding en landbouwhuisdieren op STEC. STEC is een bacterie die maag-darmklachten kan veroorzaken met symptomen variërend van diarree tot hemorragische colitis en het hemolytisch-uremisch syndroom (HUS (hemolitisch uremisch syndroom)). (1) STEC O157- en non-O157-infecties zijn meldingsplichtig onder de Wet publieke gezondheid (Wpg (Wet Publieke Gezondheid)), vanwege de ernst van de ziekte, vooral bij kleine kinderen en ouderen, en het risico op grootschalige uitbraken. In dit artikel presenteren we de resultaten van de surveillance voor het jaar 2015.
content
Auteurs: I.H.M. Friesema, S. Kuiling, M. van der Voort, P.H. in ’t Veld, M.E.O.C. Heck, W. van Pelt
Infectieziekten Bulletin: september 2016, jaargang 27, nummer 7
Methoden
Zie voor een uitgebreidere beschrijving van de methode onze eerdere publicatie. (2)
Binnen de aangifte diende in 2015 elke positieve bevinding van STEC (Shigatoxineproducerende E. coli-stammen) (op basis van fecesonderzoek of serologie) door het laboratorium gemeld te worden aan de lokale GGD (Gemeentelijke Gezondheidsdienst). Daarnaast worden de laboratoria gevraagd om mogelijk STEC positieve E. coli (Escherichia coli)-kolonies op te sturen naar het RIVM (Rijksinstituut voor Volksgezondheid en Milieu). Op het RIVM worden alle ingestuurde STEC-isolaten met behulp van polymerase chain reaction (PCR (polymerase chain reaction)) getest op de aanwezigheid van de belangrijkste virulentiegenen (shigatoxine genen (stx (shigatoxine)-genen), E. coli attaching-and-effacing gen (eae (E. coli attaching-and-effacing)-gen) en het EHEC (Enterohemorragische Escherichia coli)-hemolysine gen (EHEC-hly (hemolysin)-gen)). Als er virulentiegenen aangetoond kunnen worden, vindt vervolgens O- en H-serotypering plaats. Tenslotte worden DNA (deoxyribonucleic acid)-profielen van de STEC O157-isolaten gemaakt door middel van pulsed-field gel electroforese (PFGE (pulsed-field gel electroforese)) om zo stammen onderling met elkaar te kunnen vergelijken.
De GGD verzamelt de basisinformatie over het klinische beeld bij de patiënt en blootstelling aan bekende risicofactoren en geeft dit via Osiris, het officiële meldingsportaal, door aan het RIVM. Daarnaast wordt, waar mogelijk, een langere vragenlijst afgenomen waarin men dieper ingaat op het klinisch beeld, gebruik van de gezondheidszorg en risicofactoren. Bij een vermoeden van een bron uit levensmiddelen of contact met landbouwhuisdieren wordt contact opgenomen met de NVWA (Nederlandse Voedsel- en Warenautoriteit) voor monstername van levensmiddelen en/of bemonstering van dierlijke bronnen of omgeving voor onderzoek naar STEC, en typering van eventuele isolaten. Daarnaast onderzoekt de NVWA jaarlijks in het kader van diverse monitoringsprojecten, relevante producten op de aanwezigheid van STEC en typeert het gevonden stammen op aanwezige stx-genen, aanhechtingsgenen (eae, aggR (Transcriptional activator)+aaiC (aaic-gen)) en serotype. De methoden bij het onderzoek van de NVWA zijn gebaseerd op ISO (International Organization of Standardization) methode 13136 en de diverse typerings PCRs van het EURL-VTEC (European Union Reference Laboratory verocytotoxin-producing E. coli) (European Union Reference Laboratory verocytotoxin-producing E. coli). De methode voor de detectie van stx2f is gebaseerd op Derzelle et al.(3)
Resultaten
Patiënten
In 2015 waren 848 patiënten via de aangifte en/of het insturen van een isolaat bij het RIVM bekend (Tabel 1; Figuur 1). Van deze patiënten hadden 77 patiënten een bevestigde STEC O157-infectie en 229 een STEC non-O157-infectie, van de overige patiënten kon de infectie niet bevestigd worden in het ingestuurde isolaat (n=80) of was er geen isolaat ingestuurd (n=462). Iets meer vrouwen dan mannen hadden een STEC-infectie. Patiënten met een STEC O157- of een STEC non-O157-infectie waren jonger (beide mediaan 23 jaar) dan de patiënten met een niet getypeerde STEC-infectie (mediaan 41 jaar (geen confirmatie) en 44 jaar (alleen Osirismelding)). Bijna de helft (44%) van de patiënten met een STEC O157-infectie werd in 2015 in het ziekenhuis opgenomen (1999-2014: 31-54%), ten opzichte van rond de 20% in de andere groepen. HUS (hemolitisch uremisch syndroom) werd gemeld voor 23 patiënten, waarvan 14 kinderen (0-15 jaar) en 9 volwassenen (23-84 jaar), 35% was vrouw. Een man van 72 jaar is overleden aan een STEC O182-infectie. De piek van STEC-infecties is, evenals in voorgaande jaren, te zien in het derde kwartaal (juli-september). Dit is het sterkste voor STEC O157, maar ook zichtbaar bij de overige meldingen van STEC. Ongeveer een vijfde van de STEC-infecties is in het buitenland opgelopen. Van de patiënten waarvan bekend was of ze wel of niet in het buitenland waren geweest, had respectievelijk 25%, 17% en 22% van de STEC O157, STEC non-O157 en de overige patiënten gereisd.
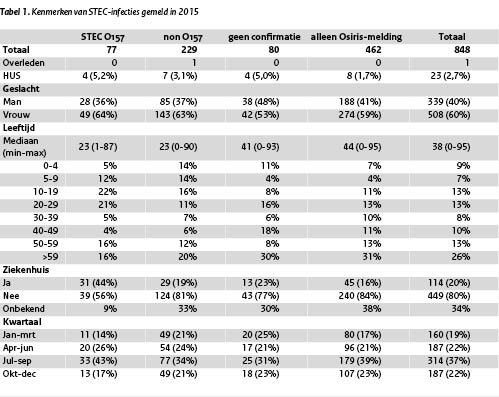
Tabel 1 Kenmerken van STEC-infecties gemeld in 2015.
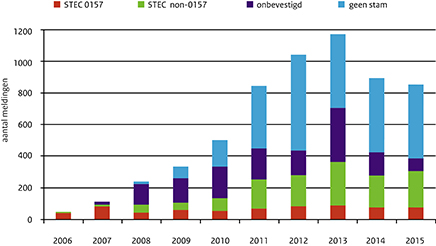
Figuur 1 Aantal STEC-infecties gemeld over de jaren 2006-2015 onderverdeeld naar STEC O157, non-O157, naar RIVM ingestuurde isolaten die niet bevestigd konden worden, en geen stam ingestuurd naar het RIVM.
Mogelijke bronnen van infectie
In 6 gevallen werden voedselmonsters in 2015 getest door de NVWA naar aanleiding van een klacht en/of een vermoede voedselbron van infectie. In de onderzochte monsters werd echter geen STEC aangetoond. Daarnaast werd in 1 geval koeienmest onderzocht als vermoedelijke bron van een O157-infectie. In dit geval werd er wel een STEC gevonden, welke geen O157 bleek te zijn (maar O182). Daarnaast onderzocht de NVWA in 2015 in 15 projecten de aanwezigheid van STEC in voedsel. Nieuw was daarbij in 2015 de screening op het stx2f-gen, welke specifiek gescreened is in kip gerelateerde-projecten. Er zijn echter in deze monitoring geen STEC-isolaten gevonden met het stx2f-gen. Wel werd in de detailhandel in 8 van de 536 monsters vers vlees (rund, varken, lam) en in 27 van 662 monsters bewerkt vlees figuur(gehakt e.d.) een STEC-isolaat gevonden. Dit komt uit op een besmetting van 3% voor vlees in de detailhandel, gelijk aan het percentage gevonden in 2014 (3%). Slechts uit 2 van de 696 monsters bewerkt pluimveevlees kreeg men een STEC-isolaat, en geen uit de 680 monsters vers pluimveevlees. In eerdere jaren onderzocht men niet het pluimveevlees op STEC. Ook in het project op exotisch vlees, in 4 van 58 partijen (5 monsters/partij), en in 3 van 65 partijen import roodvlees (5 monsters/partij) vond men STEC. Verder onderzocht de NVWA in de detailhandel 127 monsters superfoods en 302 monsters (on)gesneden groenten, waarbij het geen STEC aan kon tonen.
In de groothandel en bij import onderzocht men 57 partijen verse kruiden, 206 partijen gedroogde kruiden, 10 partijen kiemgroente, 79 partijen niet-vegetarische tapas en 171 partijen humus/tofu/tahin (alle 5 monsters/partij). Hierbij was 1 partij verse kruiden STEC positief.
Naast de projecten gericht op voedsel onderzocht men ook kippenmestmonsters (leghennen) op aanwezigheid van STEC, waarbij men in geen van de 270 geteste bedrijven (5 monsters/bedrijf) een STEC-isolaat vond. Samen met het (bijna) niet terug vinden van STEC op pluimveevlees, lijkt dit aan te geven dat pluimvee geen (belangrijke) bron is van STEC.
De analyse van de gevonden serotypen in 2015 leverde 29 verschillende O-groepen, waarbij O174 (n=7), O8 (n=6) en O91 (n=5) de meest gevonden serotypen waren. Opmerkelijk is dat men maar 2 isolaten O113 vond, waarvan men in 2014 het meest aantrof (n=12).
STEC O157
In 2015 werden 77 patiënten met een STEC O157-infectie gemeld, wat neerkomt op 0,46 per 100.000 inwoners. Dit is vergelijkbaar met 2014 (0,47), maar lager dan in 2013 (0,54) en 2012 (0,51). Drie kinderen (2, 3 en 7 jaar) en een volwassene (26 jaar) ontwikkelden in 2015 HUS (5%; 9% gemiddeld over 1999-2014).
Een ingevulde vragenlijst was beschikbaar van 43 van de 77 patiënten (56%). Binnen deze groep consumeerde 5% rauwe melk(producten), wat een daling ten opzichte van voorgaande jaren was (2011-2014: 9-15%; Figuur 2). Consumptie van rauwkost (70%) is iets gedaald ten opzichte van 2014 (77%) en 2013 (84%). Consumptie van rauw vlees (44%) blijft fluctueren en is ten opzichte van 2014 (29%) gestegen. Het contact met dieren (19%) steeg ten opzichte van 2014 (9%) en blijkt vergelijkbaar met 2010-2011 (19-21%). Contact met een andere zieke (5%) is, evenals in 2014 (3%), laag in 2015.
Van alle 77 STEC O157-patiënten was het isolaat beschikbaar, de helft bevatte alleen het stx2-gen (49%) de andere isolaten (51%) bevatten beide genen. Alle O157-isolaten bevatten het eae-gen en het EHEC-hly-gen. Drie isolaten (alle stx2 positief) waren positief voor sorbitol. Met behulp van PFGE konden 10 clusters in 2015 onderscheiden worden, 6 clusters van 2 personen, 2 clusters van 3 personen en 1 cluster van 4, respectievelijk 5 personen. Bij het cluster van 5 personen, allen volwassen vrouwen, was sprake van clustering in regio en tijd: de eerste zieke werd een kleine 3 weken voor de anderen ziek en woonde het verste weg, de andere 4 wonen in dezelfde provincie en ontwikkelden in dezelfde week klachten; de vragenlijsten leverden geen aanwijzing voor een gezamenlijke bron. Bij het cluster van 4 personen is er alleen clustering in tijd tussen de eerste 2 patiënten te zien (1 week verschil in eerste ziektedag), verder geen clustering of aanwijzingen voor een gezamenlijke bron. Eén van de clusters van ٣ personen bestaat uit een gezinscluster. Dit cluster ontstond waarschijnlijk via persoon-op-persoon transmissie gezien de tijd tussen de eerste ziektedagen, waarbij beide kinderen HUS ontwikkelden. De derde persoon kan op basis van regio, tijd en overige gegevens niet aan het gezinscluster gelinkt worden. Bij het tweede cluster van 3 personen en bij 2 clusters van 2 personen is een gezamenlijke bron mogelijk op basis van clustering in tijd, ze werden binnen deze clusters allen binnen 10 dagen tijd ziek; de beschikbare gegevens leveren echter geen aanwijzing wat de bron kan zijn geweest. Het derde cluster van 2 personen betreft een gezinscluster van moeder en dochter, waarbij de dochter HUS ontwikkelde. Bij de overgebleven 3 clusters was een gemeenschappelijke bron niet aannemelijk door de spreiding in regio en in tijd (meer dan 2 weken tussen de eerste ziektedagen).
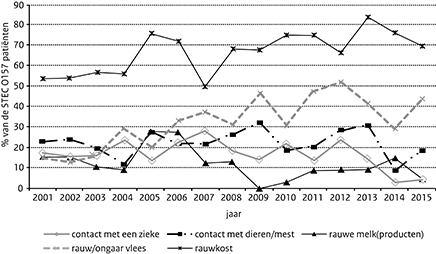
Figuur 2 Percentage STEC O157-patiënten per risicofactor per jaar (2001-2015), exclusief de STEC O157-patiënten van de uitbraken in 2005, 2007 en 2009.
STEC non-O157
Er werden in totaal 229 patiënten gemeld waarbij een STEC non-O157-infectie bevestigd kon worden. Omdat niet alle laboratoria testmethoden gebruiken waarmee je alle STEC-typen kunt detecteren, kon de incidentie niet rechtstreeks berekend worden. 17 van de 29 in 2015 insturende laboratoria (59%) gebruikten een methode waarmee je alle STEC-typen kunt detecteren. Deze laboratoria waren verantwoordelijk voor 87% van de bevestigde STEC O157-meldingen. De verhouding O157:non-O157 binnen deze laboratoria was 1:3,5. Omgerekend naar heel Nederland zou dit voor 2015 uitkomen op ongeveer 265 STEC non-O157-infecties, wat overeenkomt met een incidentie van 1,6 patiënten per 100.000 inwoners. De verhouding lag in 2008-2014 tussen 1:2,3 en 1:4,2. De incidentie van STEC non-O157 was lager dan in 2013 (2,3 patiënten per 100.000) en vergelijkbaar met 2012 (1,6 patiënten per 100.000 inwoners) en 2014 (1,7 patiënten per 100.000 inwoners).
Van de 229 patiënten hadden 38 (17%) een vragenlijst ingevuld. Contact met een andere zieke (3%) is gedaald ten opzichte van de voorgaande jaren (2008-2014: 6-22%). De consumptie van rauw vlees (37%) en contact met dieren (21%) daalden beide licht ten opzichte van 2014 (respectievelijk 43% en 27%). De consumptie van rauwkost (68%) steeg dit jaar weer iets na een daling vorig jaar (53%).
De consumptie van rauwe melk(producten) (11%) is vergelijkbaar met vorig jaar (8%).
Van de 228 beschikbare STEC non-O157-isolaten bevatten 103 (45%) isolaten alleen het stx1-gen, 79 (35%) isolaten alleen het stx2-gen (waarvan 8 (4%) het stx2f-gen) en 46 (20%) isolaten bevatten beide genen. In totaal hadden 85 (37%) isolaten het eae- en het EHEC-hly-gen, 12 (5%) isolaten hadden alleen het eae-gen, 79 (35%) isolaten alleen het e-hly-gen en 52 (23%) isolaten geen van beide genen. Van de 229 STEC non-O157-isolaten konden de labs 13 keer de O-groep niet typeerbaar en 1 maal niet getypeerd. Bij de overige 215 isolaten werden 49 verschillende O-groepen gevonden. De 3 meest gevonden O-groepen in 2015 waren O26 (n=30), O91 (n=27) en O146 (n=21). Over de gehele periode 2007-2015 waren O26 (n=156), O91 (n=130), O63 (n=82), O103 (n=80) en O146 (n=74) de 5 meest gevonden O-groepen.
Zes kinderen (0-8 jaar; STEC O26 (4x), O80 en O177) en 1 volwassene (39 jaar; STEC O182) ontwikkelden HUS in 2015. Tussen 2007 en 2015 meldde men in totaal 21 HUS-patiënten met een STEC non-O157-infectie, waarbij men alleen STEC O26 (8x) en O104 (5x, waarvan 4 ten tijde van de Duitse uitbraak in 2011) vaker dan een keer als verwekker vond. In deze periode constateerde men in Nederland nog geen HUS-gevallen gerelateerd aan STEC O91 of O146 aan.
STEC melden
In juli 2016 wijzigden de criteria voor de melding van diarree door STEC:
STEC-diarree
Elk persoon met ten minste 1 van de volgende symptomen:
- diarree
- braken
- bloed in ontlasting
en
- maximaal 21 dagen tussen de eerste ziektedag en de afnamedatum (ziekteduur was eerder geen criterium)
- in combinatie met 1 van onderstaande laboratoriumcriteria: * aantonen combinatie van stx1- plus escV-/eae-genen aantonen van stx2-gen
- aantonen (kweek) van shigatoxineproducerende E. coli
De criteria voor de melding van HUS zijn niet gewijzigd:
HUS:
Elk persoon met een plotselinge nierinsufficiëntie, gevolgd door ten minste ١ van de volgende symptomen:
- hemolytische anemie
- trombocytopenie
in combinatie met 1 van de genoemde laboratoriumcriteria:
- specifieke antilichaamresponse voor STEC-serogroepen of
- aantonen van STEC of
- aantonen van shigatoxine in feces of darminhoud of
- aantonen van het stx1-gen of het stx2-gen in feces of darminhoud
Discussie
Het aantal gemelde STEC-infecties daalde iets in 2015, net zoals in 2014. Vooral het aantal stammen dat niet bevestigd kon worden op het RIVM daalde sterk. Dit komt waarschijnlijk doordat laboratoria isolaten voorselecteren wanneer ze deze insturen naar het RIVM. Na een periode van lichte stijging van het aantal STEC O157-infecties tot 90 meldingen in 2013, is het aantal in 2015 (n=77) vergelijkbaar met 2014 (n=79). Dit is wel nog hoger dan de 32-57 meldingen in de periode 1999-2010 (met een uitschieter naar 83 meldingen door een landelijke uitbraak in 2007).
De meest getypeerde STEC non-O157-infecties in 2015 waren STEC O26, O91 en O146. Dit zijn dezelfde typen als vorig jaar. In 2015 meldde men 7 HUS-patiënten met een STEC non-O157, daarvan hadden er 4 een STEC O26. In de periode 2007-2015 ontwikkelde 5,1% van de patiënten met een STEC O26-infectie HUS. Dit is vergelijkbaar met het percentage voor O157 over dezelfde periode: 6,0%. Op basis van voorkomen en ernst is STEC O26 daarmee, na STEC O157, de belangrijkste verwekker van STEC-infecties. STEC O26 kan ernstige ziekte, inclusief HUS, veroorzaken (4-8). Gezien de recente uitbraak in Roemenië is dit nog steeds relevant (9).
In 2015 maakte men nog op lokaal of regionaal niveau pragmatische keuzes welke STEC-positieve PCR-resultaten wel en welke niet relevant zijn. Hierdoor ontstonden meldingen met alleen basisgegevens over de patiënt en bijvoorbeeld geen informatie over symptomen en risicofactoren. Bovendien werd er voor die meldingen geen isolaat naar het RIVM voor typering gestuurd. In 2013-2014 onderzocht men in 2 regio’s alle STEC-gevallen die binnen de toenmalige meldingscriteria vielen. (10) Het project bestond uit een laboratoriumdiagnostiekdeel en een GGD-deel, en had als doel om een wetenschappelijk onderbouwd laboratoriumalgoritme en richtlijnen voor meldingsplicht en bron- en contactonderzoek op te stellen. Op basis van dit onderzoek en informatie vanuit de STEC-surveillance werden nieuwe meldingscriteria opgesteld die recent zijn ingegaan. De focus van de STEC-meldingsplicht komt te liggen op acute en ernstige(re) infecties. Dit wordt bereikt door op laboratoriumniveau alleen nog isolaten die minimaal het stx2-gen of het stx1-gen samen met het eae-(of escV-)gen bevatten, meldingsplichtig te houden. Daarnaast moet de patiënt minimaal diarree, braken en/of bloed in de ontlasting hebben en moeten er maximaal 3 weken tussen eerste ziektedag en moment van ontlastingafname zitten. Toepassing van de nieuwe criteria op de meldingen van afgelopen jaren levert een totale reductie van ongeveer 60-70% ten opzichte van de oude meldingscriteria. De criteria voor het melden van HUS binnen de STEC-surveillance blijven onveranderd.
Naast de melding in Osiris werd een uitgebreidere vragenlijst over risicofactoren gebruikt binnen de surveillance. Sinds 2010 lag het percentage ingevulde vragenlijsten voor O157 tussen 43% en 63% en voor non-O157 tussen 17% en 38%. Op het moment dat de nieuwe meldingscriteria ingaan, is deze vragenlijst geïntegreerd in Osiris, waarbij je deze alleen hoeft in te vullen wanneer de infectie (waarschijnlijk) in Nederland is opgelopen. De losse vragenlijst vervalt dan.
Van de in 2015 meest voorkomende serotypen in STEC non-O157-infecties, O26, O91 en O146, werden respectievelijk maar 0, 5, en 3 isolaten gevonden in voedsel. Daarnaast, werden de door de NVWA meest gevonden serotypen, O174 en O8, ieder aangetoond bij 1 en 4 patiënten in 2015. Opmerkelijk is dat de NVWA in de onderzochte monsters, net als in 2014, geen O157-isolaten vond. Dit zou veroorzaakt kunnen worden door verandering in de onderzoeksmethode. Men past de methode die specifiek is voor de isolatie van O157 niet meer toe op onderzoek van levensmiddelen en mest. Deze is vervangen door de algemene methode voor het aantonen van STEC. De afwezigheid van de stx2f-variant in pluimveevlees en -mest laat zien dat je verder moet zoeken naar de bron van de STEC-infecties die drager zijn van deze variant.
We kunnen concluderen dat STEC O157 en STEC O26 in Nederland de belangrijkste verwekkers van STEC-infecties zijn zowel qua voorkomen als ernst. Na een aantal jaren van een stijgend aantal STEC-meldingen in Nederland, daalde dit aantal in 2014 en 2015 iets.
Dankwoord
Wij bedanken alle GGD’en en medisch microbiologische laboratoria hartelijk voor hun medewerking bij het verzamelen van de patiëntgegevens en het insturen van isolaten. Ook bedanken we de medewerkers van de NVWA voor het bemonsteren van en onderzoek naar landbouwhuisdieren en (verdacht) voedsel.
Auteurs
I.H.M. Friesema1, S. Kuiling1, M. van der Voort2,
P.H. in ’t Veld2, M.E.O.C. Heck1, W. van Pelt1
1. RIVM, Centrum Infectieziektebestrijding
2. Nederlandse Voedsel- en Warenautoriteit (NVWA), Divisie Consument en Veiligheid
Correspondentie
- Smith JL, Fratamico PM, Gunther NW. Shiga Toxin-Producing Escherichia coli. Advances in applied microbiology 2014; 86: 145-97.
- Friesema IHM, de Jager CM, Heuvelink AE (alveolaire echinokokkose), et al. Intensieve surveillance van STEC (Shigatoxineproducerende E. coli-stammen) in Nederland, 2010. Infectieziekten Bulletin 2011; 22: 370-4.
- Derzelle S, Grine A, Madic J, et al. A quantitative PCR (polymerase chain reaction) assay for the detection and quantification of Shiga toxin-producing Escherichia coli (STEC) in minced beef and dairy products. International Journal of Food Microbiology 2011; 151: 44-51.
- Bonnet R, Souweine B, Gauthier G, et al. Non-O157: H7 Stx2-producing Escherichia coli strains associated with sporadic cases of hemolytic-uremic syndrome in adults. J Clin Microbiol 1998; 36: 1777-80.
- Gould LH, Mody RK, Ong KL, et al. Increased Recognition of Non-O157 Shiga Toxin-Producing Escherichia coli Infections in the United States During 2000-2010: Epidemiologic Features and Comparison with E. coli (Escherichia coli) O157 Infections. Foodborne Pathog Dis 2013; 10: 453-60.
- Bielaszewska M, Mellmann A, Bletz S, et al. Enterohemorrhagic Escherichia coli O26:H11/H- : A New Virulent Clone Emerges in Europe. Clin Infect Dis 2013; 56: 1373-81.
- Käppeli U, Hächler H, Giezendanner N, Beutin L, Stephan R. Human infections with non-O157 Shiga toxin-producing Escherichia coli, Switzerland, 2000-2009. Emerg Infect Dis 2011; 17: 180-5.
- Caprioli A, Scavia G, Morabito S. Public Health Microbiology of Shiga Toxin-Producing Escherichia coli. Microbiology spectrum 2014; 2: EHEC (Enterohemorragische Escherichia coli)-0014-2013.
- Peron E, Zaharia A, Zota LC (Liquid chromatography), et al. Early findings in outbreak of haemolytic uraemic syndrome among young children caused by Shiga toxin-producing Escherichia coli, Romania, January to February 2016. Euro Surveill 2016; 21: 30170.
- Kooistra-Smid AMD, de Boer RF, Croughs PD, et al. Nieuw onderzoek naar diagnostiek van STEC en HUSEC (hemolytisch uremisch syndroom E. coli): STEC-ID (individuele dosis)-net. Ned Tijdschr Med Microbiol 2013; 21: 70-3.