Begin september 2015 werd door een arts-microbioloog een melding aan de GGD (Gemeentelijke Gezondheidsdienst) gedaan van een kind met een huidinfectie veroorzaakt door Staphylococcus aureus. Het kind was in het ziekenhuis opgenomen en kreeg intraveneus antibiotica toegediend. De stafylokok was Panton Valentine leucocidine (PVl)-positief. In augustus 2015 was het jongere broertje van het kind tijdens opname in het ziekenhuis ook gediagnosticeerd met een huidinfectie veroorzaakt door een PVl-positieve S.aureus. Rondom het gezin zouden nog meer mensen klachten hebben passend bij een huidinfectie die was veroorzaakt door een PVl-positieve S.aureus. Was hier sprake van een uitbraak en wat is dan het beste plan van aanpak.
mei 2016
Auteurs: M. de Jong , S.Thijsen , R. van Kessel , E. Fanoy
Infectieziekten Bulletin: mei 2016, jaargang 27, nummer 5
Het PVL (Panton-Valentine leukocidine)-gen, dat is samengesteld uit het lukS-PV (poliovirus)- en lukF-PV-gen, codeert voor een exotoxine dat celmembranen kapot maakt en zo zorgt voor toegenomen invasief vermogen. Als de bacterie het gen ‘afleest’, wint het aan bacteriële virulentie. Vooral steenpuisten zijn geassocieerd met PVl-positieve stafylokokken. In Nederland is de afgelopen jaren een toename te zien van het aantal huidinfecties met PVL-positieve meticillineresistente
Staphylococcus aureus-stammen. (1)
Bron- en contactonderzoek
De GGD (Gemeentelijke Gezondheidsdienst) startte bron- en contactonderzoek op basis van de 10 stappen van uitbraakonderzoek (2), om dit mogelijke cluster van patiënten met infecties en dragerschap van PVl-positieve S. aureus in kaart te brengen.
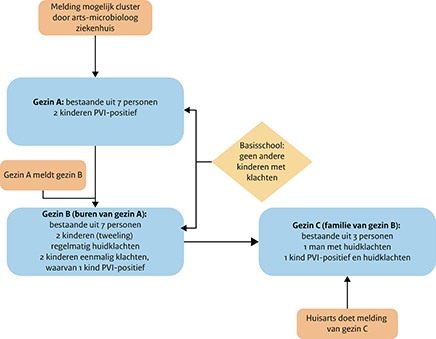
Gezin A bestond uit 2 ouders en 5 kinderen. Twee kinderen waren gediagnosticeerd met infecties veroorzaakt door PVL-positieve S. aureus-stammen. Eén van deze 2 kinderen (indexpatiënt) werd door de arts-microbioloog aan de GGD gemeld. De 2 kinderen hadden sinds begin 2015 meerdere steenpuisten en abcessen, afgewisseld met klachtenvrije perioden. De kinderen waren niet bekend met onderliggend lijden en hadden geen andere huidafwijkingen. Eén van de ouders had diabetesmellitustype-II en eczeem. De ouders hadden geen beroep waarin ze een besmettingsrisico voor anderen konden zijn, zij werkten niet in de gezondheidszorg of in een andere sector waarbij veel fysiek contact is. Het gezin had geen huisdieren.
Uit het contactonderzoek bleek dat 2 buurkinderen uit gezin B vergelijkbare huidklachten hadden. Het gezin B bestond uit 2 ouders en 5 kinderen. Twee kinderen (een tweeling) hadden om de paar maanden huidklachten, afgewisseld met klachtenvrije perioden van een aantal weken, 2 kinderen hadden 1 keer huidklachten gehad en 1 kind had nooit huidklachten gehad. Ook beide ouders hadden geen klachten gehad. De tweeling had eczeem. De andere kinderen en beide ouders hadden geen andere huidaandoeningen en waren niet bekend met onderliggend lijden. Ook deze ouders hadden geen risicoberoep. Het gezin had wel een huisdier, een hond. Bij een van de 2 kinderen die eenmalig huidklachten hadden gehad, werd begin 2015 een kweek afgenomen tijdens een ziekenhuisopname. Op verzoek van de GGD werd typeringsonderzoek gedaan waaruit bleek dat het om een PVl-positieve S. aureus ging.
Figuur 1. Cluster schematisch in kaart gebracht
Gezin C werd gemeld door een huisarts. Gezin C, familie van gezin B, bestond uit 2 ouders en een kind. De vader had op moment van melding sinds een week last van een pussende steenpuist op zijn buik. Zijn vrouw en kind hadden geen klachten. Het was niet bekend of de ouders in dit gezin een risicoberoep hadden. Ook dit gezin had een hond.
De kinderen van gezin A en gezin B speelden regelmatig buiten met elkaar en kwamen ook bij elkaar thuis. De kinderen gingen naar dezelfde basisschool. Bij navraag aan de schooldirecteur bleken er in de afgelopen maanden geen andere kinderen te zijn geweest met verdachte huidklachten.
Diagnostiek
Er werd voor gekozen om alle leden van gezin B en C via de huisarts te screenen op stafylokokkendragerschap door middel van een neus- keelkweekonderzoek. Gezin A werd niet gescreend omdat de 2 kinderen met klachten 3 en 5 maanden tevoren al gescreend waren in het ziekenhuis tijdens opname.
Binnen gezin B werden geen personen met S. aureus-dragerschap gevonden. Binnen gezin C werd bij het kind S. aureus gevonden; bij de vader werd geen S. aureus gevonden ondanks het feit dat hij 3 weken tevoren een pussende steenpuist op de buik had.
De S. aureus-stammen van de 2 kinderen uit gezin A, van 1 kind uit gezin B (waarbij al een jaar eerder kweekonderzoek was uitgevoerd in het ziekenhuis) en van het kind uit gezin C werden nader getypeerd met de amplification fragmenth lengt polymorfism (AFLP (Amplification Fragment Length Polymorphism))-techniek en met een antibiogram. Het resultaat was dat de stammen met deze methodes niet van elkaar te onderscheiden waren.
Behandeling
Op advies van de GGD startte de huisarts met stafylokkeneradicatietherapie bij alle leden van gezin A. Deze therapie bestond uit mupirocinezalf (aangebracht in de neus) en hibiscrub, gedurende 5 dagen. Gezin B werd niet behandeld omdat alle afgenomen kweken op dat moment negatief bleken en de gezinsleden bovendien geen klachten hadden. Gezin C werd ook niet behandeld omdat het kind ondanks de positieve uitslag van het kweekonderzoek, nooit huidklachten had gehad. De vader van gezin C werd behandeld met antibiotica omdat hij klachten had passend bij een PVl+ stafylokokkeninfectie.
Epidemiologisch lijkt het erop dat de transmissieroute via de kinderen was gegaan: de kinderen van gezin A en gezin B speelden regelmatig met elkaar en de gezinnen B en C waren familie.
Ruim een maand na de S.aureus-eradicatietherapie van gezin A keerden de klachten weer terug bij 1 kind. Het kind werd opgenomen in het ziekenhuis en behandeld met antibiotica. Op dat moment waren alle gezinsleden vrij van huidklachten.
Van gezin B is, op moment van het schrijven van dit artikel, onbekend of zij nog klachten hebben.
De huisarts van gezin C meldde dat het kind in dit gezin een huidinfectie kreeg na de eerdere screening waarbij zowel een S.aureus en groep A-streptokok werd aangetoond. Hiervoor werd hij niet behandeld omdat de huidinfectie niet ernstig was en de huid nagenoeg genezen was.
Discussie en conclusie
PVl-positieve stafylokokkenuitbraken onder gezinnen zijn eerder beschreven. In 2012 werd een PVl+ stafylokokkenuitbraak beschreven onder 5 gezinnen die familie van elkaar waren.(3) Deze gezinnen werden gescreend en bleken hetzelfde spa-type te hebben. De gezinsleden kwamen vaak bij elkaar. In een andere studie werd een uitbraak beschreven onder gedetineerden, waarbij 2 celgenoten allebei positief testten voor PVl-positieve (PLV+) S. aureus in opgelopen wonden. Zij deden mee aan gemeenschappelijke afdelingsactiviteiten zoals sporten, luchten en gesprekgroepen. (4) In 2006 werd een uitbraak beschreven onder de leden van een voetbalclub. (5) Een speler had een wondinfectie veroorzaakt door PVl+ stafylokokken. Daarop is bij 35 spelers uit andere teams ook kweekonderzoek gedaan. Negen van hen waren drager van PVl+ stafylokokken. Transmissie vond waarschijnlijk plaats op het veld of in de kleedkamer. Recent werd een PVl+ S.aureus-uitbraak onder streetdancers beschreven. Pas na recidiverende infectie bleek dat er een transmissiecyclus in stand gehouden werd via deze dansgroep en de GGD besloot een ruime screeningsgroep te definiëren (6).
Een infectieziekte veroorzaakt door PVl is niet meldingsplichtig. Veel mensen hebben last van steenpuisten. Hierover wordt de GGD normaliter niet geïnformeerd. Omdat in deze casus de GGD wel geïnformeerd werd, en er bovendien een reële verdenking op een cluster was, met bovendien een recidiverend karakter van de infectie, besloot de GGD actie te ondernemen. Omdat surveillance op steenpuisten, of clusters hiervan, ontbreekt is de GGD afhankelijk van alerte professionals of bezorgde burgers. Samenwerking met de (huis) arts die de GGD moet weten te vinden met dit soort problematiek en met de arts-microbioloog voor onder andere typering is essentieel om een uitbraak van huidinfecties effectief te bestrijden. Wanneer er geen aanwijzing is voor een cluster (verschillende typeringsuitslagen, dus sporadische gevallen), dan kan je het aantal mensen voor S.aureus-eradicatiebehandeling beperkt houden. Bij aanwijzing op onderlinge transmissie vanwege vergelijkbare typeringsuitslagen, is het te overwegen meer nauwe contacten ook te behandelen.
Zoals beschreven kregen 2 kinderen ondanks eerdere eradicatiebehandeling opnieuw een huidinfectie, waarschijnlijk veroorzaakt door PVl+ S.aureus. De bron van de bacteriën was niet duidelijk: mogelijk waren deze bacteriën afkomstig van de kinderen zelf, van hun naaste contacten of de woonomgeving. Ook de hond van gezin B, die niet gescreend werd, had drager kunnen zijn en dus geïncludeerd kunnen worden in screening en groepsbehandeling. De hier beschreven uitbraak toont vooral de hardnekkigheid van dit soort clusters en de relevantie om een (mogelijk herhaalde) groepsgerichte aanpak te kiezen.
Na afloop van de uitbraak gaf de huisarts voor de GGD verbeterpunten aan: ze zou prijs stellen op een contactpersoon binnen de GGD; nu kreeg ze telefonisch vaak niet direct de betrokken GGD-medewerker te pakken. Daarnaast waren er vragen van de betrokken families die wellicht met frequenter telefonisch overleg tussen GGD en de families sneller beantwoord hadden kunnen worden. Tot slot hadden de inventarisatie van contacten, kweekafnames en advisering in totaal 2 maanden in beslag genomen. Deels was dit onvermijdelijk omdat het tijd kostte om cliënten te benaderen. Ook waren niet alle contacten direct in beeld; ze druppelden binnen op basis van de gesprekken. Desondanks is het streven naar een kortere duur wenselijk, omdat dit kan leiden tot meer tevredenheid bij de betrokkenen over de genomen bestrijdingsmaatregelen.
Alhoewel de antibiogrammen van de verschillende isolaten vergelijkbaar waren, is het discriminerend vermogen van een antibiogram beperkter dan van typeringen zoals AFLP. Door deze AFLP-typering werd het onderlinge verband zeer aannemelijk. De GGD-betrokkenheid bij een verdenking op clusters of recidieven had in de hier beschreven uitbraak een duidelijke meerwaarde. Ook heeft de GGD bij PVl-stafylokokkengeassocieerde clusters een handelingsperspectief: op basis van anamneses en afname van diagnostiek kunnen de omvang van een cluster en eventuele risicofactoren beter in beeld gebracht worden. (Dragerschap)behandeling om recidivering en transmissie te doorbreken kan vervolgens, in samenspraak met (huis)arts en arts-microbioloog overwogen worden.
Auteurs
M. de Jong 1, S.Thijsen 2, R. van Kessel 3, E. Fanoy 1,4
1. GGD regio Utrecht, Zeist
2. Diakonessenhuis, Utrecht
3. Huisartsenpraktijk Van Kessel, Zeist
4. Centrum Infectieziektebestrijding, RIVM, Bilthoven
Correspondentie
Literatuur
- LCI (Landelijke coördinatie infectieziektebestrijding)-richtlijn. 2011. LCI-richtlijn Staphylococcus aureus-infecties inclusief MRSA (Methicilline-resistente Staphylococcus aureus)
- Field Epidemiology Manual (ECDC (European Centre for Disease Prevention and Control))
- W.J.M. Niessen, G.D. Mithoe, A.V.M. Moller, J. Broer, J. van der Have en A. Ott. 2015. Een cluster van MRSA-infecties bij een familie. Infectiebulletin. Jaargang 26;nr 5. Blz. 93-95.
- G.T. van den Berg, M.J.M. te Wierik. 2014. Een cluster van PVL-positieve MRSA-infecties bij gedetineerden. Infectiebulletin. Jaargang 25;nr 6. Blz. 160-163.
- A. van Lier. 2006. Cluster van PVL-positieve MRSA bij voetbalclub. Infectiebulletin. Jaargang 17;nr3. Blz.109-111.
- C.F.H. (Stijn) Raven, Peter van Wijngaarden, Gonny Moen en M.M.L. (Miranda) van Rijen; Clusteruitbraak MRSA buiten het ziekenhuis; Ned Tijdschr Geneeskd. 2014;158