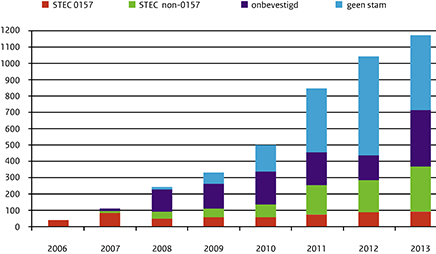
De incidentie van shigatoxineproducerende Escherichia coli (STEC (Shigatoxineproducerende E. coli-stammen))-infecties is de afgelopen jaren in Nederland langzaam gestegen. In totaal werden in 2013 1173 infecties gemeld, waarvan 90 patiënten met een STEC O157-infectie, 278 patiënten met een STEC non-O157-infectie en 805 patiënten met STEC zonder verdere bevestiging. Twintig patiënten ontwikkelden het hemolytisch-uremisch syndroom (HUS (hemolitisch uremisch syndroom)), 1 patiënt overleed aan een STEC O111-infectie.
content
Auteur(s): I.H.M. Friesema , S. Kuiling , E.G. Biesta-Peters , R. Zuidema , W.K. van der Zwaluw , M.E.O.C. Heck , W. van Pelt
Infectieziekten Bulletin: februari 2015, jaargang 26, nummer 2
Shigatoxineproducerende Escherichia coli (STEC (Shigatoxineproducerende E. coli-stammen)) is een bacterie die maagdarmklachten kan veroorzaken met symptomen variërend van diarree tot hemorragische colitis en het hemolytisch-uremisch syndroom (HUS (hemolitisch uremisch syndroom)).(1) STEC O157- en non-O157-infecties zijn meldingsplichtig onder de Wet publieke gezondheid (Wpg (Wet Publieke Gezondheid)), vanwege de ernst van de ziekte, vooral bij kleine kinderen en ouderen, en het risico op grootschalige uitbraken. Aangezien niet alle Nederlandse laboratoria technieken gebruiken die het mogelijk maken STEC non-O157 te detecteren, is dit deel van de surveillance niet landelijk dekkend. De incidentie van zowel STEC O157 als STEC non-O157 is de afgelopen jaren langzaam gestegen. De ziektelast van STEC non-O157 is meestal lager, mede afhankelijk van de specifieke O-groep. In dit artikel presenteren we de resultaten van de surveillance voor het jaar 2013.
Figuur 1. Aantal STEC-infecties gemeld over de jaren 2006-2013, onderverdeeld naar STEC O157, non-O157, naar het RIVM ingestuurde isolaten die niet bevestigd konden worden, en geen stam ingestuurd naar het RIVM.
Methoden
Binnen de Wpg dient elke positieve bevinding van STEC (op basis van fecesonderzoek of serologie) door het laboratorium gemeld te worden aan de lokale GGD (Gemeentelijke Gezondheidsdienst). Daarnaast worden de laboratoria gevraagd om mogelijk STEC-positieve E. coli-isolaten op te sturen naar het RIVM. Op het RIVM worden deze isolaten met behulp van PCR (polymerase chain reaction) (polymerase chain reaction) getest op de aanwezigheid van de belangrijkste virulentiegenen: genen coderend voor Shigatoxinetype 1 en -type 2 (stx (shigatoxine)1 en stx2), het E. coli (Escherichia coli)-attaching-and-effacing gen (eae (E. coli attaching-and-effacing)) en het EHEC (Enterohemorragische Escherichia coli)-hemolysinegen (e-hly (hemolysin)). Als er een of meer virulentiegenen aangetoond kunnen worden in een isolaat, wordt vervolgens het O- en H- serotype bepaald. Tenslotte worden dnaprofielen van de STEC O157-isolaten gemaakt door middel van PFGE (pulsed-field gel electroforese) (pulsed-field gel electroforese) om de stammen onderling met elkaar te kunnen vergelijken.
De GGD verzamelt de basisinformatie over het klinisch beeld van de patiënt en de blootstelling aan bekende risicofactoren en geeft dit via Osiris, het officiële meldingsportaal, door aan het RIVM. Daarnaast wordt, waar mogelijk, een langere vragenlijst afgenomen waarin dieper ingegaan wordt op klinisch beeld, gebruik van de gezondheidszorg en risicofactoren. Bij een vermoeden van een bron uit levensmiddelen of door contact met landbouwhuisdieren wordt contact opgenomen met de Nederlandse Voedsel en Waren Autoriteit (NVWA (Nederlandse Voedsel- en Warenautoriteit)) voor monstername van levensmiddelen, bemonstering van dierlijke bronnen of omgeving voor onderzoek naar STEC, en typering van eventuele isolaten. Zie voor een uitgebreidere beschrijving van de methode referentie (2).
Resultaten
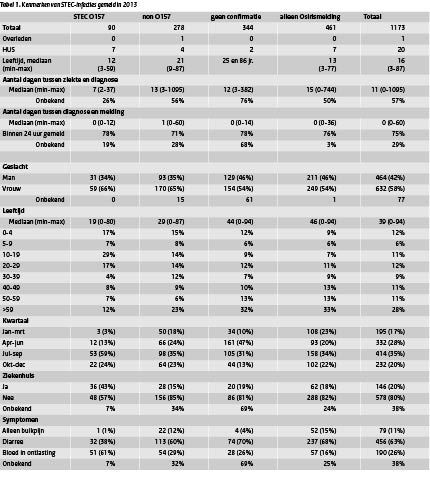
In 2013 waren 1173 patiënten via de aangifte en/of het insturen van een isolaat bij het RIVM bekend (Tabel 1). Bij 368 patiënten kon de aanwezigheid van stx-genen in de ingestuurde isolaten bevestigd en getypeerd worden (90x O157 en 278x non-O157). Een man van 61 jaar overleed aan een STEC O111-infectie. Twintig patiënten ontwikkelden HUS, waarvan 10 kinderen (3-13 jaar) en 10 volwas-
senen (19-87 jaar). Onder de patiënten met een bevestigde STEC O157-en non-O157-infectie waren meer vrouwen dan mannen, respectievelijk 66% en 65%. Bij de meldingen die niet op het RIVM bevestigd konden worden en die alleen via Osiris gemeld waren, was het verschil minder groot (54% vrouwen). De patiënten met een STEC O157-infectie waren met 19 jaar mediaan de jongste, gevolgd door patiënten met een STEC non-O157-infectie (29 jaar).
Tabel 1. Kenmerken van STEC-infecties gemeld in 2013 (klik op de tabel voor een grote weergave)
STEC O157 laat de sterkste seizoenstrend zien met 59% van de infecties in het derde kwartaal (Tabel 1). Ook bij de niet bevestigde infecties is een trend te zien, maar met de meeste infecties in het tweede kwartaal. Bijna de helft van de patiënten met een STEC O157-infectie werd in het ziekenhuis opgenomen (1999-2012: 31-54%), ten opzichte van minder dan 20% in de andere groepen. Bloed in de ontlasting komt bij STEC O157 ruim 2 keer zoveel voor (61% versus 16-29%). Hierbij moet wel worden opgemerkt dat de informatie over symptomen lang niet altijd beschikbaar was, vooral in de groep patiënten met niet bevestigde infecties. De tijdsduur tussen eerste ziektedag en de STEC-diagnose is het kortst bij patiënten met STEC O157-infecties met 7 dagen, en het langst bij de groep patiënten waarvan geen isolaat ingestuurd is (14 dagen). Echter, deze data waren maar voor 74% (STEC O157) en 50% (geen isolaat) van de patiënten beschikbaar. In driekwart van de gevallen werd de melding aan de GGD binnen 24 uur na diagnose gedaan.
Mogelijke bronnen van infectie
In een onbekend aantal gevallen was er contact tussen GGD en NVWA over de mogelijke bron van infectie. In 1 geval resulteerde dit in een inspectie van een bedrijf maar was er geen aanleiding om monsters te nemen voor verder onderzoek. Bij een gezinscluster van vader en dochter, waarbij de dochter HUS ontwikkelde, werden tijdens de inspectie wel een aantal voedselmonsters onderzocht. Alle monsters waren negatief.
Uit de reguliere surveillanceprogramma’s en importcontroles van de NVWA konden uit circa 90 unieke partijen van voornamelijk vleesproducten isolaten worden verkregen die getypeerd konden worden. Omdat uit een aantal partijen meerdere STEC-isolaten werden geïsoleerd, kwam het totaal aantal typeerbare STEC-isolaten in 2013 op 120: 29 isolaten bevatten alleen het stx1-gen, 72 isolaten alleen het stx2-gen en 13 isolaten bevatten beiden. Zes isolaten bevatten alleen het eae-gen. In 2013 werden 51 verschillende serotypes aangetroffen, waarbij O8 (n=14), O113 (n=13), O100 (n=7) en O174 (n=7) de meest gevonden serotypes waren.
STEC O157
In 2013 werden 90 patiënten met een STEC O157-infectie gemeld, wat neerkomt op 0,54 per 100.000 inwoners. Dat is opnieuw een stijging ten opzichte van voorgaande jaren: 32-85 patiënten per jaar of 0,22-0,51 patiënten per 100.000 inwoners sinds 1999, exclusief de landelijke uitbraken. Vier kinderen en 3 volwassenen ontwikkelden in 2013 HUS (8%, 10% gemiddeld over 1999-2012).
Een ingevulde vragenlijst was beschikbaar van 55 van de 90 patiënten (61%). Binnen deze groep had 84% rauwkost gegeten, wat een stijging is ten opzichte van voorgaande jaren (2008-2012: 67-75%). Consumptie van rauw vlees (42%) is juist weer iets minder vaak genoemd (2012: 52%, 2011: 48%; 2008-2010: 31-46%). Bijna een derde van de patiënten (31%) had contact met dieren (2008-2012: 19-32%) en 15% had voorafgaand contact met een andere zieke gehad (2008-2012: 14-24%). Consumptie van rauwe melk(producten) was over 2011-2013 constant met 9-10% (2008-2010: 0-13%).
Van 87 van de 90 STEC O157-patiënten waren isolaten beschikbaar, 2 (2%) daarvan bevatten alleen het stx1-gen, 34 (39%) bevatten alleen het stx2-gen, en 49 isolaten bevatten beide genen (56%). Alle O157-isolaten bevatten het H7-gen. Eén isolaat (stx1-positief) was sorbitolpositief. Tenslotte bevatten 86 isolaten het eae-gen en alle het e-hly-gen.
Met behulp van PFGE konden 11 clusters in 2013 onderscheiden worden, variërend van 2 tot 6 isolaten per cluster die afkomstig waren van eenzelfde aantal personen. Bij 3 clusters (2 patiënten, 4 patiënten en 5 patiënten) was een gemeenschappelijke bron niet aannemelijk door de spreiding in tijd en regio, en bij het vierde cluster had een van beide patiënten de infectie in Turkije opgelopen. Bij 4 clusters (3x 2 patiënten, 1x 3 patiënten) was sprake van een sterke clustering in tijd met maximaal 2 dagen verschil in eerste ziektedag, met uitzondering van 1 van de patiënten uit het cluster van 3 patiënten. Regionaal was er hierbij echter geen sprake van clustering en de vragenlijsten leveren geen aanwijzing voor een bron. Eén cluster van 2 patiënten liet een clustering in tijd (6 dagen verschil), regio, leeftijd (54 en 60 jaar) en geslacht (man) zien, maar van 1 van beide was geen verdere informatie beschikbaar. Het tiende cluster bestond uit 6 patiënten die allemaal in een periode van 4 weken ziek waren geworden. De eerste patiënt had de infectie mogelijk in Malta opgelopen. Van 5 van de 6 patiënten was een vragenlijst beschikbaar. Daarin viel op dat ze allemaal sla hadden gegeten en degenen die een verdere specificatie hadden gegeven, hadden rucola (2x) of gemengde sla (1x) gegeten. Toch was het twijfelachtig of het de sla was geweest, gezien de houdbaarheid van sla en de periode van bijna 4 weken waarin de patiënten ziek waren geworden. Het laatste cluster bestond uit 2 kinderen uit 1 gezin. Van 2 patiënten met 2 O157-isolaten bleken de PFGE-patronen niet identiek te zijn.
STEC non-O157
Er werden in totaal 278 patiënten gemeld waarbij een STEC non-O157-infectie bevestigd kon worden. Aangezien niet alle laboratoria testmethodes gebruiken waarmee alle STEC gedetec-
teerd kunnen worden, kan de incidentie niet rechtstreeks berekend worden. Negentien van de 31 insturende laboratoria (61%) gebruikten een methode waarmee alle STEC gedetecteerd kan worden. Deze laatste laboratoria waren verantwoordelijk voor 73% van de bevestigde STEC O157-meldingen. De verhouding O157: non-O157 binnen deze laboratoria is 1:4,2. Omgerekend naar heel Nederland zou dit voor 2013 uitkomen op ongeveer 380 STEC non-O157-infecties wat correspondeert met een incidentie van 2,3 patiënten per 100.000 inwoners. De verhouding lag in 2008-2012 tussen 1:2,3 en 1:3,6. De incidentie van STEC non-O157 is daarmee ook gestegen ten opzichte van de voorgaande jaren: 1,6 patiënten per 100.000 inwoners (2012) tegen 0,7-1,4 per 100.000 inwoners (2008-2011).
Er waren ingevulde vragenlijsten van 54 van de 278 patiënten (19%). Binnen deze groep had 78% rauwkost gegeten (2008-2012: 67-85%). Consumptie van rauw vlees (35%) werd minder vaak genoemd (2008-2012: 42-62%). Contact met dieren fluctueert sterk met 15% in 2013 en tussen 9-48% in 2008-2012. Ook consumptie van rauwe melk(producten) fluctueert sterk en was 15% in 2013 (2008-2010: 6-31%). Contact met een andere zieke voor zelf ziek te worden bleef vergelijkbaar laag met 2012 (6%) ten opzichte van 2008-2011 (8-22%).
Bij 277 van de 278 STEC non-O157-isolaten waren gegevens over de virulentiegenen beschikbaar: 139 (50%) isolaten bevatten alleen het stx1-gen, 80 (29%) isolaten alleen het stx2-gen (waarvan 21 (8%) het stx2f-gen) en 58 (21%) isolaten bevatten beide genen. In totaal 96 (35%) isolaten hadden het eae- en het e-hly-gen, 27 (10%) isolaten hadden alleen het eae-gen, 84 (30%) isolaten alleen het e-hly-gen en 70 (25%) isolaten geen van beide genen. Van de 278 STEC non-O157 isolaten was 19 keer de O-groep niet typeerbaar en 2 keer was deze autoagglutinabel. Bij de overige 257 isolaten werden 59 verschillende O-groepen gevonden. De 3 meest gevonden O-groepen waren O26 (n=35), O91 (n=31) en O103 (n=24). Over de gehele periode (2007-2013) zijn O26 (n=105), O91 (n=85), O63 (n=68), O103 (n=53) en O113 (n=43) de 5 meest gevonden O-groepen. Twee kinderen en 2 volwassenen ontwikkelden HUS, veroorzaakt door infecties met respectievelijk STEC O26 en O8, en O87 en O104.
Discussie
Het aantal gemelde STEC-infecties is in 2013 opnieuw gestegen. De stijging is voornamelijk te zien bij de niet-getypeerde STEC-infecties - dat zijn infecties die gemeld waren via Osiris maar zonder ingestuurd isolaat en isolaten die op het RIVM niet bevestigd konden worden - en de STEC non-O157 infecties, wat het gevolg is van de invoering van de STEC-PCR. Ook het aantal meldingen van STEC O157-infecties is de afgelopen jaren gestegen van 32-57 meldingen in de periode 1999-2010 (met een uitschieter naar 83 meldingen door een landelijke uitbraak in 2007) naar 90 meldingen in 2013. Mogelijk dat ook deze stijging, hoewel veel kleiner dan bij de andere STEC-infecties, wordt veroorzaakt door de invoering van de STEC-PCR. Door de stijging van het aantal meldingen werden voornamelijk op lokaal of regionaal niveau, pragmatische keuzes gemaakt welke STEC-positieve PCR-resultaten wel en welke niet relevant zijn. Dit uit zich in meldingen met alleen basisgegevens over de patiënt en bijvoorbeeld geen informatie over symptomen en risicofactoren, en meldingen zonder dat een isolaat naar het RIVM voor typering werd gestuurd. Op dit moment loopt er een project in 2 regio’s, waarvan een deel laboratoriumdiagnostiek en een deelGGD, om een wetenschappelijk onderbouwd keuzealgoritme op te stellen en vervolgens waar nodig richtlijnen voor meldingsplicht en broncontactonderzoek aan te passen. De resultaten van het project worden binnenkort verwacht.(3)
In de afgelopen jaren zagen we in de surveillance een relatief grote groep STEC-infecties waarbij de bacterie het stx2f-gen bezat. STEC-stammen met dit gen waren nog amper in de literatuur beschreven. Analyse van de Nederlandse data gebruikmakend van 87 STEC non-O157 infecties met het stx2f-gen over de jaren 2008-2011, liet zien dat stx2f STEC-infecties over het algemeen milder verlopen dan een infectie met een STEC non-O157 of STEC O157. (4) Echter, in 2013 ontwikkelde een negenjarige jongen, zonder onderliggend lijden, HUS waarbij een O8:H19 stx2f STEC werd gevonden. (5) Het absolute aantal STEC non-O157 infecties met het stx2f-gen is in 2013 gelijk gebleven aan 2012 (21 isolaten). De tot nu toe in de Nederlandse STEC-surveillance gedetecteerde STEC O63 bezit altijd het stx2f-gen en stond de afgelopen 3 jaar altijd in de top 3 van meest voorkomende STEC non-O157 infecties. In 2013 is STEC O63 gezakt naar een gedeelde zevende plaats met 10 isolaten. Het enige serotype dat sinds 2007 altijd één van de meest gevonden STEC non-O157 types was, is STEC O26. Dit serotype heeft de potentie om ernstige ziekte, inclusief HUS, te veroorzaken. (6-11) Maar ook STEC O91 en O103, de 2 andere meest gevonden serotypes in 2013 en in de top 5 over de periode 2007-2013, hebben deze potentie. In Europa zijn de serotypes O26, O91 en O103, de top 3 in Nederland in 2013, ook de 3 meest gerapporteerde serotypes na STEC O157.(12) Over het algemeen werden door de NVWA andere serotypes in voedsel aangetroffen dan in de surveillance bij patiënten. De enige die bij beide vrij regelmatig gezien wordt, is STEC O113, waarbij het aan de voedselkant om vlees ging.
Uit de vergelijking van de ingevulde vragenlijsten van de patiënten met die van personen uit de algemene bevolking (13) kunnen risicofactoren worden bepaald. Uit de gegevens van 2008-2012 blijkt dat de consumptie van rauwe vleesproducten (filet amé-ricain en ossenworst) de belangrijkste risicofactor voor STEC O157-infectie was. Voor STEC non-O157-infecties waren dit contact met landbouwhuisdieren (patiënten jonger dan 10 jaar) en de consumptie van rundvlees (patiënten van 10 jaar en ouder). (14)
Geconcludeerd wordt dat STEC non-O157-infecties in Nederland klinisch beduidend minder belangrijk zijn dan STEC O157-infecties, maar wel vaker voorkomen. Niet alleen het aantal STEC-meldingen in Nederland maar ook de voor dekking gecorrigeerde incidentie is gestegen ten opzichte van voorgaande jaren. De meest getypeerde STEC non-O157-infecties in 2013, STEC O26, O91 en O103, zijn alle 3 serotypes die, evenals STEC O157, ernstige ziekte kunnen veroorzaken.

Auteurs
I.H.M. Friesema 1, S. Kuiling 1, E.G. Biesta-Peters 2, R. Zuidema 1, W.K. van der Zwaluw 1, M.E.O.C. Heck 1, W. van Pelt 1
1. Centrum Infectieziektebestrijding , RIVM, Bilthoven
2. Laboratorium Voeder- en Voedselveiligheid, Nederlandse Voedsel en Warenautoriteit, Wageningen
Correspondentie
Ingrid.friesema@rivm.nl
- Smith JL, Fratamico PM, Gunther NWt. Shiga Toxin-Producing Escherichia coli. Advances in applied microbiology 2014; 86: 145-97.
- Friesema IHM, de Jager CM, Heuvelink AE (alveolaire echinokokkose), et al. Intensieve surveillance van STEC (Shigatoxineproducerende E. coli-stammen) in Nederland, 2010. Infectieziekten Bulletin 2011; 22: 370-4.
- Kooistra-Smid AMD, de Boer RF, Croughs PD, et al. Nieuw onderzoek naar diagnostiek van STEC en HUSEC (hemolytisch uremisch syndroom E. coli): STEC-ID (individuele dosis)-net. Ned Tijdschr Med Microbiol 2013; 21: 70-3.
- Friesema I, van der Zwaluw K, Schuurman T, et al. Emergence of Escherichia coli encoding Shiga toxin 2f in human Shiga toxin-producing E. coli (Escherichia coli) (STEC) infections in the Netherlands, January 2008 to December 2011. Euro Surveill 2014; 19: pii=20787.
- Friesema IHM, Keijzer-Veen MG, Koppejan M, et al. A case of hemolytic uremic syndrome associated with Escherichia coli O8:H19 harboring the Shiga toxin 2f gene. Emerg Infect Dis 2014; (accepted).
- Bonnet R, Souweine B, Gauthier G, et al. Non-O157: H7 Stx2-producing Escherichia coli strains associated with sporadic cases of hemolytic-uremic syndrome in adults. J Clin Microbiol 1998; 36: 1777-80.
- Gould LH, Mody RK, Ong KL, et al. Increased Recognition of Non-O157 Shiga Toxin-Producing Escherichia coli Infections in the United States During 2000-2010: Epidemiologic Features and Comparison with E. coli O157 Infections. Foodborne Pathog Dis 2013; 10: 453-60.
- Mellmann A, Fruth A, Friedrich AW, et al. Phylogeny and disease association of Shiga toxin-producing Escherichia coli O91. Emerg Infect Dis 2009; 15: 1474-7.
- Bielaszewska M, Mellmann A, Bletz S, et al. Enterohemorrhagic Escherichia coli O26:H11/H- : A New Virulent Clone Emerges in Europe. Clin Infect Dis 2013; 56: 1373-81.
- Rosales A, Hofer J, Zimmerhackl LB, et al. Need for Long-term Follow-up in Enterohemorrhagic Escherichia coli-Associated Hemolytic Uremic Syndrome Due to Late-Emerging Sequelae. Clin Infect Dis 2012; 54: 1413-21.
- Käppeli U, Hächler H, Giezendanner N, Beutin L, Stephan R. Human infections with non-o157 Shiga toxin-producing Escherichia coli, Switzerland, 2000-2009. Emerg Infect Dis 2011; 17: 180-5.
- ECDC (European Centre for Disease Prevention and Control). Annual epidemiological report. Reporting on 2011 surveillance data and 2012 epidemic intelligence data. Stockholm: ECDC, 2013.
- Friesema IHM, van Gageldonk-Lafeber AB, Van Pelt W. Extension of traditional infectious disease surveillance with a repeated population survey. Eur J Public Health 2014; doi: 10.1093/eurpub/cku122.
- Friesema IHM, Schotsborg M, Heck MEOC, Van Pelt W. Risk factors for sporadic Shiga toxin-producing Escherichia coli O157 and non-O157 illness in The Netherlands, 2008-2012. Epidemiol Infect 2014; doi: 10.1017/S0950268814002349.