Een mogelijke relatie tussen Clostridium perfringens en het Sudden Infant Death Syndrome was de aanleiding om de aanwezigheid van Clostridium perfringens in poedervoeding op zuigelingen voor de Nederlandse markt te onderzoeken. In 2 van de 51 onderzochte verpakkingen is Clostridium aangetoond, waarvan in 1 verpakking C. perfringens. Sequentieanalyse toonde aan dat er sprake was van intrinsieke besmetting van het poeder in de verpakking. Clostridium bleek niet homogeen in de verpakking te zijn verdeeld en de besmetting was lager dan 10 kve (kolonievormende eenheden)/gram product. Aanwezigheid van Clostridium in poedervoeding zou door de zuivelsector en babyvoedingproducenten, als een een potentieel risico, moeten worden geïmplementeerd in de borging van de voedselveiligheid.
content
Auteurs: E.G. Biesta-Peters, M. Oral, J.G. van der A.
Infectieziekten Bulletin, jaargang 25, nummer 7, augustus 2014
De aanwezigheid van Clostridium spp (species).-sporen in poedervoeding voor zuigelingen heeft in de zomer van 2013 veel publiciteit gehad door een incident in Nieuw Zeeland. De publiciteit was niet alleen vanwege de mogelijke gezondheidsrisico’s voor de zuigelingen, maar ook de mogelijke economische gevolgen voor de Nederlandse zuivelindustrie. (1) Poedervoeding voor zuigelingen is geen steriel product en het productieproces en de fysiologische kenmerken van dit product maken dat de eventueel aanwezige micro-organismen kunnen overleven in het poeder. Of de aanwezige micro-organismen zich uiteindelijk kunnen vermeerderen in het poeder hangt af van de bereiding- en bewaaromstandigheden. Er is een gezondheidsrisico voor de zuigelingen indien de omstandigheden na bereiding groei van micro-organismen toelaten en de fysieke toestand van het kind niet optimaal is. (2-6) Voor babymelkpoeder en andere gedroogde poedervormige producten voor speciale medische toepassingen bij baby’s jonger dan 6 maanden zijn dan ook voedselveiligheidscriteria met betrekking tot Salmonella spp. en Cronobacter spp. opgenomen in Verordening (EG (Europese Gemeenschap)) 2073/2005. Daarnaast is er in deze verordening voor poedervoeding voor zuigelingen een proceshygiënecriterium vastgesteld met betrekking tot de aanwezigheid van Enterobacteriaceae. (7)
Clostridium spp. in poedervoeding voor zuigelingen wordt in diverse wetenschappelijke artikelen genoemd als mogelijk voedselveiligheid risico. (2,8-11) Daarnaast lijkt er een relatie maar geen oorzakelijke verband te zijn tussen het voorkomen van Clostridium perfringens in de darmen van baby’s en het Sudden Infant Death Syndrome (SIDS (sudden infant death syndrome)). Melkpoeder dat Clostridium perfringens of sporen daarvan bevat wordt gezien als oorzaak van de blootstelling van baby’s aan dit micro-organisme. (9-11) Toch zijn voor dit micro-organisme geen productspecifieke criteria vastgesteld. Op nationaal niveau is vastgelegd in het Warenwetbesluit Bereiding en Behandeling van Levensmiddelen, dat pathogene micro-organismen en hun toxinen in eet- en drinkwaren afwezig moeten zijn in hoeveelheden die schadelijk kunnen zijn voor de volksgezondheid. Clostridium perfringens is specifiek benoemd in art.4, lid 1 onder d.; hiervoor geldt dat eet- en drinkwaren niet meer dan 105 kweekbare Clostridium perfringens per gram of milliliter mag bevatten. (12)
Omdat er geen productspecifieke eisen gesteld zijn aan de aanwezigheid van Clostridium spp. in poedervormige zuigelingenvoeding worden er door de Nederlandse Voedsel en Waren Autoriteit (NVWA (Nederlandse Voedsel- en Warenautoriteit)) geen monsters in het kader van toezicht op naleving van wetgeving onderzocht. Ook is deze product- en parametercombinatie niet opgenomen in recente monitoring- en surveillance projecten van de NVWA en zijn voorgangers. In opdracht van Bureau Risicobeoordeling en Onderzoeksprogrammering (BuRO (Bureau Risicobeoordeling & Onderzoeksprogrammering)) van de NVWA is een oriënterend onderzoek uitgevoerd naar de aanwezigheid van Clostridium perfringens in poedervoeding voor zuigelingen verkrijgbaar op de Nederlandse markt. Dit artikel beschrijft de resultaten van het onderzoek.
Materiaal en Methoden
Voor dit onderzoek is van september tot en met november 2013 willekeurig bemonsterd in winkels en is getracht zoveel mogelijk verschillende merken en productiebatches melkpoeder voor baby’s te bemonsteren. Monsters zijn tot het moment van onderzoek bij kamertemperatuur en donker bewaard.
De inhoud van de verpakkingen is onderzocht op de aanwezigheid van Clostridium perfringens met behulp van 2 verschillende methodes: een telling van het aantal aanwezige micro-organismen conform ISO (International Organization of Standardization) (Internationale Organisatie voor Standaardisatie) 7937:2004 (13) en een aan-/afwezigheidtest van Clostridium perfringens waarbij de ophoping is uitgevoerd conform ISO 6461-1 (14) en de bevestigingsreacties conform ISO 7937:2004 (13). Dit betekent dat voor de telling van het aantal Clostridium perfringens in het poeder een decimale verdunningsreeks gemaakt werd van 10 gram van het monster. De 10-1 - en 10-2 -verdunningen werden 20 ± 2 uur bij 37±1°C anaeroob geïncubeerd in een gietplaat met Sulfiet Cycloserine (SC) agar en een deklaag van SC-agar. Na bebroeden werden de zwarte tot grijs-zwarte kenmerkende of verdachte kolonies bevestigd door middel van een beweeglijkheidtest, het testen van de nitraatreductie, lactose fermentatie en gelatinevervloeing. Clostridium perfringens is niet beweeglijk, kan nitraat reduceren, bij lactoseomzetting treedt zuurvorming en gasvorming op en er is sprake van gelatinevervloeiing. Voor de aan-/afwezigheidtest van Clostridium perfringens werd 10 gram monster opgelost in 100 ml Differential Reinforced Clostridial Medium (DCRM) en gedurende 48 ± 2 uur bebroed bij 37±1°C. Wanneer na bebroeden de inhoud van de potten zwart was verkleurd, was de ophoping verdacht en werd een entoog materiaal van de ophoping afgestreken op SC-agar. De SC-agar werd anaeroob bebroed bij 37±1°C gedurende 20 ± 2 uur. Kenmerkende en/of verdachte kolonies werden bevestigd zoals eerder beschreven.
Bij de start van het project was alleen een methode voor de telling van Clostridium perfringens beschikbaar conform de ISO-methode. Omdat er lage aantallen Clostridium perfringens werden verwacht is besloten om ook een methode te ontwikkelen voor het aantonen van Clostridium perfringens door middel van ophopen en deze methode beperkt te valideren. De ophopingmethode zoals hierboven beschreven is beperkt gevalideerd door zowel het medium als het medium met matrix, poedervoeding voor zuigelingen, te besmetten met een reeks verdunningen van Clostridium perfringens in een Pepton Fysiologisch Zout (PFZ)oplossing en zo de aantoonbaarheidsgrens van de methode te bepalen. Incubatie, isolatie en bevestiging werden uitgevoerd zoals hierboven beschreven.
Wanneer verdachte kolonies biochemisch bevestigd waren als Clostridium perfringens zijn ze verder geïdentificeerd met behulp van API 20A (BioMerieux, 2011) volgens de instructies van de fabrikant en aanvullend getest op de aanwezigheid van toxinegenen zoals beschreven in Tansuphasiri, 2001. (15) Er werd getest op het gen PLC, coderend voor fosfolipase C - ook wel α-toxine genoemd. Dit wordt geproduceerd door alle Clostridium perfringens-stammen en op het gen CPE (Carbapenemase-producerende enterobacterales), coderend voor Clostridium perfringens-enterotoxine. Detectie van de genen vond plaats door amplificatie met behulp van een duplex PCR (polymerase chain reaction) gevolgd door gelelectroforese.
Gevonden isolaten en de positieve controle Clostridium perfringens die gedurende het onderzoek zijn gevonden en gebruikt, zijn onderling vergeleken op verwantschap door de isolaten te sequencen met het CPE-gen als target en de resultaten te analyseren met behulp van CLC Genomics WorkBench 6.5.1- software.
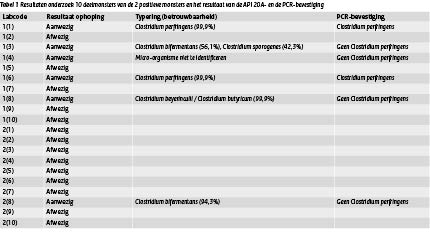
Tabel 1 Resultaten onderzoek 10 deelmonsters van de 2 positieve monsters en het resultaat van de API 20A- en de PCR-bevestiging
Klik op de tabel voor een grote weergave
Resultaten
Er zijn in de periode 1 september 2013 tot 15 november 2013 in totaal 51 melkpoedermonsters onderzocht. Deze zijn zowel met de ophopingmethode als met de tellingmethode onderzocht op de aanwezigheid van en aantallen Clostridium perfringens. De aantoonbaarheidsgrens voor de ophopingmethode is vastgesteld op 1 kve (kolonievormende eenheden)/10 g product. Er was geen effect van de matrix, melkpoeder, op de aantoonbaarheidsgrens van Clostridium perfringens waarneembaar.
In geen van de monsters is Clostridium perfringens met behulp van een directe telling aangetoond, maar in 2 monsters is wel Clostridium perfringens aangetoond met behulp van de ophopingmethode. Beide positieve monsters zijn nogmaals onderzocht door uit elke positieve verpakking 10 monsters van 10 gram te onderzoeken op de aanwezigheid van Clostridium perfringens. De resultaten per deelmonster en de extra bevestiging van het isolaat met behulp van API 20A en PCR zijn weergegeven in tabel 1. Voor monster 1 waren 5 van de 10 ophopingen opnieuw positief en voor monster 2 was 1 van de 10 ophopingen opnieuw positief. Het isolaat van monster 2 bleek zowel met de API 20A- als de PCR-bevestiging geen Clostridium perfringens te zijn maar Clostridium bifermentans. De isolaten van monster 1 bleken in 2 gevallen Clostridium perfringens te zijn en de overige isolaten waren Clostridium bifermentans/Clostridium sporogenes, Clostridium beyerincuiii/Clostridium butyricum of hadden geen typeerbaar profiel. Het blijkt dus bij besmetting om besmetting met gemixte cultures te gaan en er kunnen meerdere Clostridium-typen in een monster voorkomen.
Sequentieanalyse van de 2 positieve isolaten uit monster 1 en de gebruikte controlestam toonde aan dat de 2 gevonden Clostridium perfringens-isolaten identiek waren en dat de controlestam en de isolaten niet identiek waren. Er was dus daadwerkelijk sprake van een intrinsieke besmetting van het poeder in de verpakking.
Discussie en conclusie
Om meer inzicht te krijgen in het voorkomen van Clostridium perfringens heeft monstername van verpakkingen met poedervoeding voor zuigelingen plaatsgevonden. Hierbij zijn zoveel mogelijk verpakkingen van verschillende producenten en batches bemonsterd. Deze monsters zijn onderzocht op de aanwezigheid van Clostridium perfringens. Van 2 van de in totaal 51 onderzochte monsters is aangetoond dat er sprake was van een Clostridium spp.-besmetting. Omdat er in eerste instantie van uit is gegaan dat de besmetting homogeen verdeeld zou zijn is er een steekproef genomen van 1 keer 10 gram monster per product voor alle 51 onderzocht producten. Uit dit onderzoek blijkt echter dat de besmetting niet homogeen verdeeld was. Bij het meerdere keren bemonsteren van dezelfde verpakking bij een positieve verpakking, bleek dat deelmonsters niet altijd positief waren. Bij monster 1 was 50% van de deelmonsters positief, bij monster 2 slechts 10%. Er is dus een reële kans op vals- negatieve resultaten in de onderzochte monsters waarbij slechts 1 deelmonster is onderzocht en er kan dus sprake zijn van een onderrapportage van het aantal besmette verpakkingen met Clostridium spp. in dit artikel.
Door alle deelmonsters van de positieve verpakkingen aanvullend te bevestigen met behulp van API 20A en PCR bleek wel dat het biochemisch reactiepatroon zoals beschreven in ISO 7937:2004 niet specifiek genoeg is voor Clostridium perfringens; ook andere Clostridium-typen werden op basis van het biochemisch reactiepatroon bevestigd als Clostridium perfringens, maar bleken dat later door bevestiging met API 20A en PCR niet te zijn. De conclusie of iets wel of niet een Clostridium perfringens was, was uniform voor de API 20A-bevestiging en voor de PCR-bevestiging. Een uitbreiding van de bestaande ISO met een aanvullende bevestigingsreactie lijkt dus noodzakelijk om vals-positieve uitslagen te voorkomen, wat vooral van belang is wanneer er op de aanwezigheid van dit micro-organisme gehandhaafd moet worden door een bevoegde autoriteit.
Omdat beide positieve monsters zowel op aantoonbaarheid als telling zijn ingezet en er geen Clostridium perfringens geteld is, valt te concluderen dat de aanwezige hoeveelheid Clostridium perfringens in de positieve monsters lager geweest moet zijn dan 10 kve/g product of dat Clostridium perfringens niet homogeen verdeeld is over de verpakking zoals eerder wel verondersteld, waardoor het deelmonster voor de ophopingmethode wel positief was en het deelmonster voor de telling negatief was. In relatie tot de hypothese dat SIDS voor kan komen door aanwezigheid van Clostridium perfringens kan in ieder geval worden gesteld dat de gevonden resultaten geen aanleiding geven om van regelmatige aanwezigheid uit te gaan. De besmettingen zijn laag en niet homogeen verdeeld in het monster. De norm voor Clostridium perfringens van maximaal 105 kweekbare Clostridium perfringens per gram of milliliter eet- en drinkwaren kan wel onderwerp van discussie zijn. Onderzoek heeft aangetoond dat de aanwezige micro-organismen in poedervoeding voor zuigelingen zich kunnen vermeerderen, hoewel dit wel afhankelijk is van de bereiding- en bewaaromstandigheden. Er is een gezondheidsrisico voor de zuigelingen indien de omstandigheden na bereiding groei van micro-organismen toelaten, indien het aantal micro-organismen een infectueuze dosis heeft bereikt en de fysieke toestand van het kind niet optimaal is. (2, 3, 4 5,6) Daarom zou het vaststellen van voedselveiligheidscriteria voor Clostridium spp. voor babymelkpoeder en andere gedroogde poedervormige producten voor speciale medische toepassingen bij baby’s jonger dan 6 maanden, zoals nu al het geval is met betrekking tot Salmonella spp. en Cronobacter spp., het overwegen waard zijn. Naast de discussie over een acceptabele norm, dient er echter ook meer inzicht te komen in de virulentie van de stammen en hun mogelijke relatie met SIDS.
Een korte inventarisatie van literatuur om de resultaten van het NVWA-onderzoek in perspectief te plaatsen leverde 4 relevante artikelen op. Zowel een ILSI (International Life Sciences Institute)-rapport (2) als Forsythe et al. (4,5) rapporteren de aanwezigheid van Clostridium in melkpoeder, hoewel Forsythe de link tussen de aanwezigheid van Clostridium en ziekte van baby’s niet waarschijnlijk acht. Brett et al. (16) rapporteren echter een geval van ziekte, maar het betreft hier Clostridium botulinum en geen Clostridium perfringens. Onderzoek uit het Verenigd Koninkrijk beschreef dat 7 van de 9 commerciële babymelkpoedermonsters Clostridium-sporen bevatte; het ging hier om Clostridium sporogenes en Clostridium butyricum. (1) Er is dus in geen van de onderzoeken een relatie tussen de aanwezigheid van Clostridium perfringens en ziekte.
Er kan worden geconcludeerd dat van de onderzochte monsters (n=51) 2 monsters Clostridium bevatten (3,9%) en dat er slechts in 1 monster (2,0%) sprake was van Clostridium perfringens-besmetting. Het huidige biochemische bevestigingspatroon, zoals beschreven in ISO 7937:2004, blijkt niet voldoende om Clostridium perfringens te kunnen onderscheiden van andere Clostridium-typen en een aanpassing van de norm lijkt dan ook wenselijk. De besmetting van het monster met Clostridium perfringens was lager dan 10 kve/gram product en er kan geen relatie worden gelegd tussen de aanwezigheid van Clostridium perfringenss en ziekte door de consumptie van poedervoeding voor zuigelingen. De geïsoleerde stam bleek namelijk niet te beschikken over het gen voor productie van Clostridium perfringens-enterotoxine en er is geen infectieve dosis bekend die zou kunnen leiden tot ziekte. Over het algemeen kan worden gesteld dat het aantal onderzochte monsters te klein is om hieruit verstrekkende conclusies te kunnen trekken. De resultaten geven echter wel aanleiding om de normen voor poedervoeding voor zuigelingen nader te bestuderen en verder onderzoek te doen naar het voorkomen van Clostridium in deze poedervoeding. In de zuivelsector, vooral bij de producenten van poedervoeding voor baby’s, dient aandacht te worden gevraagd voor de mogelijke aanwezigheid van Clostridium perfringens in deze producten. Het zou door de producenten, niet als een urgent maar wel als een potentieel risico, moeten worden geïmplementeerd in de borging van de voedselveiligheid.

Auteurs
E.G. Biesta-Peters, M. Oral, J.G. van der A, Laboratorium Voeder- en Voedselveiligheid, Nederlandse Voedsel en Waren Autoriteit, Wageningen.
Correspondentie
- Veldman, J. W., 2013, China legt import melkpoeder Nieuw-Zeeland stil. via www.boerderij.nl/Rundveehouderij/Nieuws/2013/8. Geraadpleegd op 20 december 2013.
- Beuchat, L., E. Komitopoulou, R. Betts, H. Beckers, F. Bourdichon, H. Joosten, S. Fanning, and B. ter Kuile. 2011. Persistence and survival of pathogens in dry foods and dry food processing environments. ILSI (International Life Sciences Institute) Europe Report Series.
- Daha, T. 2005. Poedervormige zuigelingenvoeding. Tijdschrift voor Hygiëne en Infectiepreventie nr.5 via http://www.rivm.nl/Documenten_en_publicaties/Algemeen_Actueel/Uitgaven/…. Geraadpleegd op 12 maart 2014
- Forsythe, S. J. 2005. Enterobacter sakazakii and other bacteria in powdered infant milk formula. Maternal & Child Nutrition. 1:44-50.
- Forsythe, S. J. 2009. Bateriocidal preparation of powdered infant formula. FSA (Food and Safety Authority) Project B13010 via http://www.foodbase.org.uk//admintools/reportdocuments/395-1-697_b13010…. Geraadpleegd op 12 maart 2014
- Kandhai, M. C., M. W. Reij, M. van Schothorst, L. G. M. Gorris, and M. H. Zwietering. 2010. Inactivation rates of Cronobacter spp (species). and selected other bacterial strains in powdered infant formulae stored at different temperatures. Journal of Food Protection 73:839-848.
- EU (Europese Unie) (2005). Verordening (EG (Europese Gemeenschap)) Nr. 2073/2005 van de Commissie van 15 november 2005 inzake microbiologische criteria voor levensmiddelen.
- Barash, J. R., J. K. Hsia, and S. S. Arnon. 2010. Presence of soil-dwelling Clostridia in commercial powdered infant formulas. The Journal of Pediatrics. 156:402-408.
- Blackwell, C. C., A. E. Gordon, V. S. James, D. A. C. MacKenzie, M. Mogensen-Buchanan, O. R. El Ahmer, O. M. Al Madani, K. Törö, Z. Csukás, P. Sótonyi, D. M. Weir, and A. Busuttil. 2001. The role of bacterial toxins in Sudden Infant Death Syndrome (SIDS (sudden infant death syndrome)). International Journal of Medical Microbiology. 291:561-570.
- Murrell, W. G., B. J. Stewart, C. O’Neill, S. Siarakas, and S. Kariks. 1993. Enterotoxigenic bacteria in the sudden infant death syndrome. Journal of Medical Microbiology. 39:114-127.
- Townsend, S., J. Caubilla Barron, C. Loc-Carrillo, and S. Forsythe. 2007. The presence of endotoxin in powdered infant formula milk and the influence of endotoxin and Enterobacter sakazakii on bacterial translocation in the infant rat. Food microbiology. 24:67-74.
- Ministerie VWS (Ministerie van Volksgezondheid, Welzijn en Sport) (2012). Warenwetbesluit Bereiding en behandeling van levensmiddelen. 9 mei 2012.
- ISO (International Organization of Standardization) 7937. 2004. Microbiology of food and animal feeding stuffs — Horizontal method for the enumeration of Clostridium perfringens — Colony-count technique
- ISO 6461-1. 1986. Water quality - Detection and enumeration of the spores of sulfite-reducing anaerobes (clostridia) - Part 1: Method by enrichment in a liquid medium
- Tansuphasiri, U. 2001. Development of duplex PCR (polymerase chain reaction) assay for rapid detection of enterotoxigenic isolates of Clostridium perfringens. Southeast Asian Journal of Tropical Medicine and Public Health. 32:105-113.
- Brett, M. M., J. McLauchlin, A. Harris, S. O’Brien, N. Black, R. J. Forsyth, D. Roberts, and F. J. Bolton. 2005. A case of infant botulism with a possible link to infant formula milk powder: evidence for the presence of more than one strain of Clostridium botulinum in clinical specimens and food. Journal of Medical Microbiology. 54:769-776.