Infectie met een buiten het ziekenhuis opgelopen meticillineresistente Staphylococcus aureus (MRSA (Methicilline-resistente Staphylococcus aureus)) treft voornamelijk jonge, gezonde mensen, zonder risicofactoren voor MRSA samenhangend met de gezondheidszorg. Patiënten komen vaak met huidinfecties en infecties van de weke delen. Op de afdeling Spoedeisende hulp (SEH (Spoedeisende Hulp)) zagen wij een 18-jarige vrouw met recidiverende abcederende huidinfecties. Zij bleek MRSA-positief. Binnen een half jaar ontwikkelden 2 personen in haar omgeving ook een MRSA-infectie. Kweken toonden community acquired - buiten het ziekenhuis opgelopen - MRSA (CA-MRSA) aan met eenzelfde typering (spa t008). Aanvullend ringonderzoek onder huisgenoten en vrienden toonde bij nog 4 personen dragerschap aan voor MRSA, waarbij 2 van hen ook overeenkomende huidinfecties hadden. Een clusteruitbraak van CA-MRSA vraagt om een gecoördineerde aanpak van zowel behandelend arts als GGD (Gemeentelijke Gezondheidsdienst). De keuze van het aanvullend ringonderzoek onder contacten was bepalend voor het doorbreken van verdere transmissie en re-infectie binnen dit cluster.
content
Auteurs: C.F.H. Raven, P. van Wijngaarden, G. Moen ,M.M.L. van Rijen
Infectieziekten Bulletin, jaargang 25, nummer 7, augustus 2014
Een clusteruitbraak van CA-MRSA (Methicilline-resistente Staphylococcus aureus) komt in Nederland relatief weinig voor. Er is sprake van een cluster wanneer tenminste 2 personen uit een groep mensen die mogelijk met elkaar te maken hebben, een infectie hebben met CA-MRSA. Zo’n cluster moet gemeld worden bij de GGD (Gemeentelijke Gezondheidsdienst). Doordat de patiënten zich vaak bij verschillende dokters melden, is een uitbraak soms moeilijk te herkennen.
In deze casuïstiek beschrijven wij een uitbraak van CA-MRSA onder vriendinnen. Wij beschrijven vervolgens de melding bij de GGD, het contactonderzoek en het beleid volgens de richtlijn van de Landelijke Coördinatie Infectieziektebestrijding (LCI (Landelijke coördinatie infectieziektebestrijding)) van het RIVM, Staphylococcus aureus-infecties, inclusief MRSA.(1)
Ziektegeschiedenissen
Patiënte A, een gezonde vrouw van 18 jaar, werd gezien op de SEH (Spoedeisende Hulp) in verband met een spontaan ontstane ontsteking van de huid bij de hiel. Punctie leverde geen pus op en patiënte werd behandeld met amoxicillineclavulaanzuur oraal. Twee dagen later namen wij haar op voor incisie en drainage van een inmiddels groot abces. Een wondkweek toonde MRSA aan. We stopten de behandeling met amoxicillineclavulaanzuur en gaven geen verdere antibiotische behandeling. Risicofactoren voor MRSA-dragerschap, waaronder opname in een buitenlands ziekenhuis en contact met levende varkens of vleeskalveren, waren bij navraag afwezig. Een maand later meldde ze zich weer op de SEH met een abcederende ontsteking, waarna nog 2 keer drainage van een huidabces op de buik werd uitgevoerd.
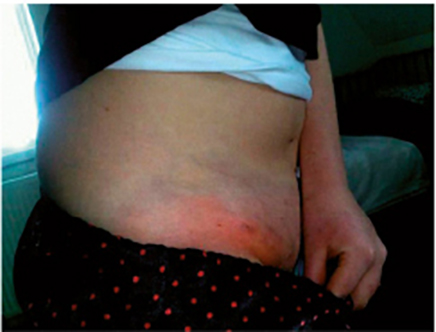
Foto 1 Patiënte A met met huidinfecties
Tijdens een vervolgcontact op de MRSA-polikliniek, 1 week later, vertelde patiënte A dat zij deel uitmaakt van een streetdancing-dansgroep. Een vriendin in dezelfde dansgroep had mogelijk last van soortgelijke huidinfecties. Zij wisselden geen handdoeken uit. Wél droegen ze soms elkaars danskleding, meestal schoongewassen, een enkele keer gedragen. De internist adviseerde de leden van de dansgroep die huidinfecties hadden contact op te nemen met hun huisarts voor diagnostiek naar MRSA.
Om de MRSA bij patiënte A te elimineren, werd zij gedurende 1 week behandeld met combinatietherapie, bestaande uit rifampicine, doxycycline en mupirocineneuszalf. Daarnaast kreeg zij hygiënische adviezen over het verschonen van kleding, nachtkleding en beddengoed in combinatie met dagelijks douchen van het hele lichaam met betadineshampoo gedurende de behandeling. Na de behandeling waren 3 sets controlekweken die om de week waren afgenomen, negatief.
Ook kweekonderzoek bij de huisgenoten van patiënte A was negatief voor MRSA. Desondanks kreeg patiënte A in de daaropvolgende 2 maanden opnieuw 2 abcederende huidinfecties (zie foto 1). Deze infecties versterkten het vermoeden dat de dansgroep een rol speelde in het onderhouden van de infectiecyclus.
Patiënte B, een 25-jarige vrouw uit dezelfde dansgroep als patiënte A, kwam bij de huisarts om zich te laten testen op MRSA, 6 maanden na patiënte A. Zelf had ze geen klachten, maar haar vriend had sinds kort regelmatig abcederende huidontstekingen, waarvoor de huisarts 2 keer antibiotica voorschreef zonder effect. Haar kweek toonde MRSA aan.
Patiënt C, een 22-jarige vrouw, was een vriendin van patiënte B en maakte geen deel uit van de dansgroep. Zij had een enkelabces. Haar huisarts kweekte het wondvocht op MRSA; de test was positief. Het type MRSA kwam overeen met het type van patiënte B (tabel 1).(2)
Het microbiologisch laboratorium meldde de infectie van patiënte C bij de GGD. Na overleg met de afdeling Medische microbiologie volgde een contactonderzoek naar MRSA. De GGD testte 10 personen rondom de 3 vrouwen (patiënten A, B en C). De ouders van patiënte B waren positief voor MRSA-dragerschap. Dit gold ook voor de vriend van patiënte B en de broer van deze vriend, bij wie uit wondinfecties ook MRSA werd gekweekt. Tabel 1 geeft een overzicht van de geteste personen. We behandelden alle MRSA-positieve personen met orale antibiotica, mupirocineneuszalf en betadineshampoo. Bij iedereen was de eradicatiebehandeling effectief en bleven de controlekweken negatief.
Opnieuw besmet
Patiënte A was gedurende een half jaar na haar laatste behandeling negatief voor MRSA. Ze ontwikkelde daarna opnieuw een abces in haar oksel, waaruit MRSA werd gekweekt. Wederom namen we MRSA-kweken af bij haar huisgenoten, zonder resultaat. Bij navraag bleek patiënte A nog contact te hebben gehad met patiënte B, voordat patiënte B behandeld was. Na een tweede antibioticabehandeling van patiënte A traden er geen infecties meer op. Tot op heden zijn haar controlekweken negatief.
Tabel 1 Kenmerken van patiënt A, B en C, mogelijke transmissiewegen en contacten met MRSA (MLVA (Multi-Locus Variable number of tandem repeat Analysis)-type/cluster (240/8)*, spa-type (t008)† en PVL (Panton-Valentine leukocidine)-positief)
Klik op de tabel voor een grote weergave
Beschouwing
De afgelopen jaren zijn in Nederland uitbraken van MRSA buiten het ziekenhuis beschreven rondom sportactiviteiten en in een schoonheidssalon.(3,4) Deze uitbraken kenden een gemeenschappelijke transmissieroute via intensief (huid)contact of gedeeld gebruik van persoonlijke bezittingen die in contact kwamen met de huid. De casus hierboven toonde eenzelfde soort uitbraak. Een dergelijke clusteruitbraak van CA-MRSA vraagt om een gecoördineerde aanpak door zowel behandelaar als GGD.
Klinische verschijnselen en behandeling
Een purulente infectie van huid of weke delen is de meest voorkomende klinische presentatie van een CA-MRSA.(5,6) Pantonvalentineleukocidine (PVL) is een belangrijke virulentiefactor, die is geassocieerd met necrotiserende fasciitis en necrotiserende pneumonie. Deze factor was aanwezig bij alle in dit cluster beschreven patiënten. De behandeling van een MRSA-infectie van de huid of weke delen kan naast chirurgische drainage bestaan uit behandeling met orale antibiotica. Voor de behandelschema’s voor MRSA-dragerschap verwijzen wij naar de betreffende richtlijnen van de Stichting Werkgroep Antibioticabeleid (http://www.swab.nl/)
Meldplicht
Sinds 2008 is een cluster van MRSA-infecties (≥ 2 personen) met klinische verschijnselen en een gemeenschappelijke transmissieroute buiten het ziekenhuis, meldingsplichtig. Doordat MRSA-patiënten zich bij verschillende behandelaren melden, kan het in de praktijk moeilijk zijn om een clusteruitbraak te herkennen. Daarom is er door de GGD en het ziekenhuis in de regio van deze uitbraak een vragenlijst opgesteld. Na elke positieve MRSA-uitslag gaat de ziekenhuishygiënist of de GGD met deze lijst na of er sprake is van een eventueel cluster.
Bron- en contactonderzoek
In een studie uit 2010 kwam overdracht van MRSA van een MRSA-positieve persoon naar een huisgenoot in ongeveer de helft van de gevallen voor. (8) Het advies is om met kweekonderzoek eventueel dragerschap bij huisgenoten te inventariseren alvorens de indexpatiënt met klinische verschijnselen te behandelen.(7)
In onze casus was aanvankelijk 1 persoon MRSA-positief (patiënte A). Pas na de positieve MRSA-uitslagen van patiënten B en C was er sprake van een meldingsplichtig cluster, dat om een uitgebreider contactonderzoek vroeg. Het onderzoek werd afgebakend rondom huisgenoten en contacten in de vriendenkring die bijpassende klachten hadden. Door afwezigheid van klachten bij de overige leden van de dansgroep en het beperkte fysieke contact onderling, werd deze groep niet meegenomen in het contactonderzoek. Tabel 2 laat zien welke personen volgens de LCI-richtlijnen in aanmerking komen voor een contactonderzoek. Wij zijn hiervan afgeweken door aansluitend op het eerder genoemde advies uit de studie alle huisgenoten te onderzoeken en niet alleen diegenen die in de gezondheidszorg werkten, zoals tabel 2 adviseert.
Tabel 2 Aanvullend contactonderzoek bij een MRSA-cluster in de openbare gezondheidszorg (bron: RIVM) Klik op tabel voor grotere weergave
Conclusie
Hoewel er buiten de bekende risicogroepen weinig MRSA voorkomt in de Nederlandse bevolking, kunnen clusters van CA-MRSA voorkomen buiten het ziekenhuis.(9,10) Houd rekening met een mogelijk cluster van MRSA rondom de MRSA-positieve patiënt bij een recidief van een MRSA-infectie na eradicatiebehandeling. In dit geval was contactonderzoek door de GGD noodzakelijk, gevolgd door eradicatiebehandeling van de MRSA-positieve contacten, om hardnekkige re-infectie en verdere transmissie in dit cluster te doorbreken.
Leerpunten
- Buiten het ziekenhuis opgelopen MRSA-infecties (CA-MRSA) uiten zich meestal door een purulente infectie van huid of weke delen. Het treft voornamelijk jonge, gezonde mensen. Denk ook aan MRSA wanneer eerstelijnsantibiotica geen effect hebben op huidinfecties of infecties van de weke delen.
- Een cluster van CA-MRSA is soms lastig te herkennen. Het vraagt om alertheid en zo nodig een actief testbeleid van de behandelaar in samenwerking met de GGD.
- Een recidief van CA-MRSA na eradicatiebehandeling kan een aanwijzing zijn voor een clusteruitbraak van CA-MRSA.
- Voordat de MRSA-positieve patiënt behandeld wordt, moeten alle gezinscontacten van de patiënt getest worden op MRSA, onafhankelijk van al dan niet aanwezige risicofactoren voor een infectie met S. aureus.
Dit artikel is eerder gepubliceerd in het Nederlands Tijdschrift voor Geneeskunde. Ned Tijdschr Geneeskd. 2014;158:A6812
Auteurs
C.F.H. Raven 1, P. van Wijngaarden 2, G. Moen 2 ,M.M.L. van Rijen 2
1. GGD West-Brabant, Breda
2. Amphia Ziekenhuis, Breda
Correspondentie
- LCI (Landelijke coördinatie infectieziektebestrijding)-richtlijn. Staphylococcus aureus-infecties, inclusief MRSA (Methicilline-resistente Staphylococcus aureus). Bilthoven: RIVM; 2011.
- Schouls LM, Spalburg EC (European Commission), Van Luit M, et al. Multiple-locus variable number tandem repeat analysis of Staphylococcus aureus: comparison with pulsed-field gel electrophoresis and spa-typing. PLoS (Plos One) ONE. 2009;4:e5082 Medline. doi:10.1371/journal.pone.0005082
- Lier A. Een cluster van PVL (Panton-Valentine leukocidine) Positieve Community Acquired MRSA. Infectieziekten Bulletin. 2006;17:109-11.
- Morroy G, Renders NHM, Timen A. Een cluster van PVL-positieve community associated-MRSA rond een schoonheidsspecialiste. Infectieziekten Bulletin. 2007;18:232-3.
- David MZ (metabole ziekten), Daum RS (respiratoir syncytieel). Community-Associated Methicillin-Resistant Staphylococcus aureus: Epidemiology and Clinical Consequences of an Emerging Epidemic. Clin Microbiol Rev. 2010;23:616-87 Medline. doi:10.1128/CMR.00081-09
- Patel M. Community-associated meticillin-resistant Staphylococcus aureus infections: epidemiology, recognition and management. Drugs. 2009;69:693-716 Medline. doi:10.2165/00003495-200969060-00004
- Optimaliseren van het antibioticabeleid in Nederland XII. Herziening SWAB richtlijn Behandeling MRSA dragers. Nijmegen: Stichting Werkgroep Antibioticabeleid; 2012.
- Mollema FP, Richardus JH, Behrendt M, et al. Transmission of methicillin resistant Staphylococcus aureus to household contacts. J Clin Microbiol. 2010;48:202-7 Medline. doi:10.1128/JCM.01499-09
- Donker GA, Deurenberg RH, Driessen C, Sebastian S, Nys S, Stobberingh EE. The population structure of Staphylococcus aureus among general practice patients from The Netherlands. Clin Microbiol Infect. 2009;15:137-43 Medline. doi:10.1111/j.1469-0691.2008.02662.x
- Den Heijer CD, Van Bijnen EM, Paget WJ, et al. Prevalence and resistance of commensal Staphylococcus aureus, including meticillin-resistant S aureus, in nine European countries: a cross-sectional study. Lancet Infect Dis. 2013;13:409-15 Medline. doi:10.1016/S1473-3099(13)70036-7
Zie ook
- Inhoud Infectieziekten Bulletin 25(7) 2014
- Infectieziekten Bulletin
- Tabel 1 Kenmerken van patiënt A, B en C, mogelijke transmissiewegen en contacten met MRSA (MLVA-type/cluster (240/8)*, spa-type (t008)† en PVL-positief)
- Tabel 2. Aanvullend contactonderzoek bij een MRSA-cluster in de openbare gezondheidszorg