Om te evalueren of druggebruikers in de Amsterdam Cohort Studie (ACS (amsterdamse cohortstudie)) nog steeds risico lopen op hiv (humaan immunodeficientievirus), hebben we trends in de hivincidentie en injecterend en seksueel risicogedrag van 1986 tot 2011 geanalyseerd. Tevens is in 2010 een soascreening (op chlamydia, gonorroe en syfilis) gedaan. Onder de 1298 deelnemers van de ACS, die een totale follow-up van 12.921 persoonsjaren (PJ) hadden, daalde de hivincidentie van 6/100 PJ in 1986 tot minder dan 1/100 PJ na 1997. Zowel het injecterend als seksueel risicogedrag daalden significant over de tijd. Van de 197 deelnemers aan de soascreening bleken slechts 5 personen (2,5%) een soa (seksueel overdraagbare aandoening) te hebben. In multivariabele analyse bleek het hebben van een vaste partner geassocieerd met onbeschermde seks. Hivgeïnfecteerde deelnemers rapporteerden minder onbeschermde seks dan deelnemers die niet met hiv geïnfecteerd waren. Deze bevindingen duiden op een gering risico op besmetting met hiv en soa. Dit suggereert dat druggebruikers geen significante rol meer spelen in de huidige verspreiding van hiv in Amsterdam.
content
Auteur(s): E.Fanoy
Infectieziekten Bulletin, jaargang 24, nummer 10, december 2013
Druggebruikers hebben een verhoogde kans om met hiv (humaan immunodeficientievirus) geïnfecteerd te raken door injecterend en seksueel risicogedrag. (1,2) Waar voorheen injecterend risicogedrag geassocieerd was met de meeste hivinfecties, lijkt nu seksueel risicogedrag een steeds grotere rol te spelen in het oplopen van hiv onder druggebruikers. (3,4) Bovendien is er een overlap tussen de transmissieroutes (injecterend) druggebruik en seksueel risicogedrag. Zo is het gebruik van bijvoorbeeld cocaïne geassocieerd met een verhoogde kans op onbeschermde seks (1), en hebben prostituees die (ooit) drugs injecteerden vaker onbeschermde seks en meer risico op soa (seksueel overdraagbare aandoening) dan prostituees die nooit drugs hebben geïnjecteerd. (3,5) Vanaf de jaren ’80 hebben harmreductionprogramma’s zich gericht op het verminderen van de risico’s van injecterend druggebruik door middel van methadonverstrekking en spuitomruil. De stabilisatie of zelfs afname van de hivincidentie onder druggebruikers in Nederland wordt toegeschreven aan deze harmreductionprogramma’s. (6,7) In Amsterdam werd een afname van injecterend risicogedrag geconstateerd tussen 1986 en 2005. (8) Echter, het seksueel risicogedrag bleef substantieel en werd beschouwd als de belangrijkste risicofactor voor het oplopen van hiv.
Om te evalueren of druggebruikers nog steeds risico lopen op hiv, hebben we tussen 1986 en 2012 trends in hivincidentie, injecterend en seksueel risicogedrag van druggebruikers in de ACS (amsterdamse cohortstudie) geanalyseerd. Om te beoordelen of interventies nodig zijn om seksueel risicogedrag te verminderen, hebben we tevens deel-nemers die een bezoek brachten aan de ACS in 2010 en 2011 getest op soa en hebben we determinanten van onbeschermde seks onderzocht.
Methoden
Studiepopulatie
De ACS onder druggebruikers (www.amsterdamcohortstudies.org) werd opgericht in december 1985. De werving heeft zich in de afgelopen jaren vooral gericht op jonge druggebruikers. Geschat wordt dat 15% van de Amsterdamse injecterende druggebruikers heeft deelgenomen aan de ACS. (9) Elke 4 (tot 2003) tot 6 maanden (vanaf 2003) keerden de deelnemers terug voor een vervolgbezoek. Bij elk bezoek werden gestandaardiseerde vragenlijsten afgenomen met betrekking tot sociaaldemografische gegevens, (injecterend) druggebruik, seksueel risicogedrag en soa. Bij het eerste bezoek werd gevraagd naar risicogedrag tijdens de afgelopen 6 maanden; bij vervolgbezoeken naar risicogedrag in de periode sinds het vorige bezoek.
Alle ACS-deelnemers die tussen november 2010 en juni 2011 voor een studiebezoek kwamen kregen een soascreening aangeboden. Deelnemers die de screening ondergingen worden in dit artikel aangeduid als ‘recente bezoekers’. Deze recente bezoekers werden getest op Chlamydia trachomatis (CT), Neisseria gonorrhoeae (NG) en Treponema pallidum (syfilis). Urinemonsters (mannen) en zelf afgenomen vaginale swabs (vrouwen) werden op CT en NG getest, serum op syfilis. Deelnemers met een verhoogd risico op soa (bijvoorbeeld symptomen hadden die bij een soa passen, gewaarschuwd waren voor een soa, prostituees, mannen die seks hebben met mannen) werden direct verwezen naar de soapolikliniek van de GGD (Gemeentelijke Gezondheidsdienst) van Amsterdam voor uitgebreide screening. (19)
Laboratoriummethoden
Bij elk studiebezoek werd serum getest op hivantistoffen (Ag/Ab Combo test, Axsym; Abott Laboratoria en bioMérieux, Frankrijk). Positieve monsters werden bevestigd met een immunoblot (Line Immuno Assay, Inno-Lipa HIV (humaan immunodeficientievirus) I/II Score; Innogenetics NV, Gent, België). Voor 2004 werden positieve monsters bevestigd met een Western blot.
Bij de recente bezoekers werden urinemonsters (mannen) en vaginale swabs (vrouwen) getest op CT en NG met de Nucleic Acid Amplification Test (NAAT) (Gen-probe Aptima Combo 2 Assay, San Diego, CA, VS (Verenigde Staten)). Serum werd getest op syfilis (Treponema pallidum particle agglutination assay; Serodia-TPPA (Treponema pallidum passive particle agglutination); Fujirebio Europa BV). Om syfilis te bevestigen en te classificeren werden reactieve monsters verder getest met de Venereal Disease Research Laboratory (VDRL (Venereal Disease Research Laboratory)) test (Wellcome, Dartford, VK). Positieve testresultaten werden geclassificeerd als ‘infectieuze syfilis’ (TPPA ≥1:80 en VDRL ≥1:8) of ‘behandelde syfilis’ (TPPA ≥1:80 en VDRL >1:1).
Laboratoriumprocedures voor deelnemers met een verhoogd risico zijn elders beschreven. (20) Samenvattend, alle recente hoogrisicodeelnemers werden getest op CT, NG en syfilis; de mannelijke tevens op niet-specifieke urethritis (NSU) en vrouwen op Trichomonas vaginalis (TV).
Behandeling van soa
Deelnemers aan de soascreening kregen schriftelijk bericht van negatieve testuitslagen. Positieve testuitslagen werden mondeling teruggekoppeld door de arts van de ACS. Ze werden vervolgens behandeld onder supervisie van dermatologen van de GGD-soapolikliniek.
Statistische analyses
Om trends in hivincidentie onder alle druggebruikers die bij intrede in de ACS hivnegatief waren te onderzoeken, werd de geobserveerde hivincidentierate per kalenderjaar berekend door het aantal geobserveerde hivseroconversies te delen door het aantal geobserveerde persoonsjaren. De datum van hivseroconversie werd geschat als de datum tussen het laatste hivnegatieve en het eerste hivseropositieve ACS-bezoek. Trends in hivincidentie per kalenderjaar onder alle druggebruikers (inclusief injecterende druggebruikers) en onder injecterende druggebruikers werden apart gemodelleerd.
Met logistische regressie werden trends in zelfgerapporteerd injecterend en seksueel risicogedrag, het gebruik van spuitomruil en het hebben van soa onder de hivnegatieve deelnemers gemodelleerd. Door gebruik te maken van generalised estimating equations (GEE), werd er gecorrigeerd voor herhaalde waarnemingen (bezoeken) per individu. We definieerden onbeschermde seks als geen (of niet altijd) gebruik van een condoom bij vaginale of anale seks. Hierover was informatie beschikbaar vanaf 1991. Met behulp van natural cubic splines werden trends in risicogedrag en hivincidentie als vloeiende curves weergegeven. (10) We gebruikten logistische regressie om determinanten voor onbeschermde seks onder de recente bezoekers van de soascreening te identificeren. Gegevens van bezoekers die de afgelopen 6 maanden geen vaginale of anale seks rapporteerden, werden niet in deze analyse meegenomen. Vanaf 2009 werd onbeschermde seks per partnertype gerapporteerd. Er is onderscheid gemaakt in 4 partnertypes: vaste partner, losse partner, prostituant en prostituee. GEE werd gebruikt om rekening te houden met het feit dat sommige deelnemers verschillend risicogedrag bij verschillende typen partners rapporteerden. (11) Een P-waarde <0.05 werd beschouwd als statistisch significant. De statistische analyses werden uitgevoerd met SPSS (Statisch computerprogramma)-software (versie 19.0, SPSS Inc.) en R statistical computing environment (versie 2.14.0; http://www.R-project.org/).
Resultaten
Demografie
Van december 1985 tot december 2011 zijn 1658 druggebruikers geregistreerd bij de ACS, waarvan 1298 met minstens 2 bezoeken. De totale followuptijd bedroeg 12.921 persoonsjaren (PJ); de mediane followuptijd was 9,2 jaar (interkwartielbereik (IKB) 3,7-14,8). Bij intrede was de mediane leeftijd 30 jaar (IKB 26-35), 62% was van het mannelijk geslacht en 71% had een Nederlandse nationaliteit (tabel 1). Het aantal druggebruikers dat jaarlijks terugkeerde voor een followupbezoek was met 94% (IKB 92-96%) stabiel over de jaren. Tot 31 december 2011 zijn 464 druggebruikers overleden.
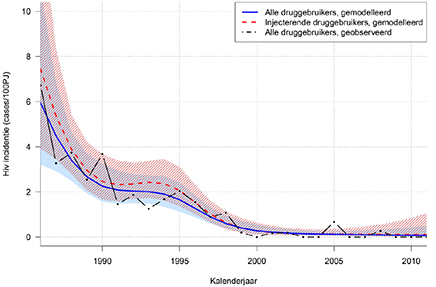
Figuur 1 Geobserveerde en gemodelleerde hivincidentie in de Amsterdam Cohort Studies onder druggebruikers, voor alle druggebruikers en voor injecterende druggebruikers, 1986-2011. De schaduw en gearceerde gebieden zijn de 95% betrouwbaarheidsintervallen voor respectievelijk alle druggebruikers (gemodelleerd) en de injecterende druggebruikers (gemodelleerd). PJ: persoonsjaren
Figuur 1 Geobserveerde en gemodelleerde hivincidentie in de Amsterdam Cohort Studies onder druggebruikers, voor alle druggebruikers en voor injecterende druggebruikers, 1986-2011. De schaduw en gearceerde gebieden zijn de 95% betrouwbaarheidsintervallen voor respectievelijk alle druggebruikers (gemodelleerd) en de injecterende druggebruikers (gemodelleerd). PJ: persoonsjaren
Hivincidentie
Bij intrede bleken 261 (20%) van de 1298 druggebruikers met hiv geïnfecteerd te zijn. Gedurende follow-up seroconverteerden 97 deelnemers voor hiv. De mediane leeftijd op het moment van hivseroconversie was 33 jaar (IKB 28-38); 59% was man en 80% had de Nederlandse nationaliteit. Het aantal hivnegatieve druggebruikers in follow-up nam toe van 133 in 1986 tot 598 in 2001, en daalde daarna tot 284 in 2011. Figuur 1 laat de geobserveerde hivincidentierates zien van alle druggebruikers en de gemodelleerde hivincidentie rates voor alle druggebruikers en voor injecterende druggebruikers alleen. De hivincidentierate onder alle druggebruikers was hoog in 1986: 5,96/100 PJ (95% betrouwbaarheidsinterval (BI) 3,21-11,05), maar deze daalde daarna significant tot minder dan 1/100 PJ vanaf 1997 (P<0,001). Onder injecterende druggebruikers was de gemodelleerde hivincidentierate in 1986 hoger 7,47/100 PJ (95% BI 3,94-14,16) en daalde ook tot minder dan 1/100 PJ vanaf 1997 (P<0,001).
Injecterend druggebruik en seksueel risicogedrag
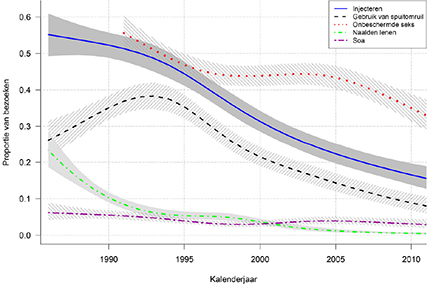
Figuur 2 toont geschatte trends in injecterend druggebruik en seksueel risicogedrag van 1986 tot 2010. Ondanks enige variatie over de tijd is er een drastische daling van injecterend druggebruik en van de prevalentie van het delen van naalden (P <0,001 voor beide, trend test). Tot 1993 nam spuitomruil toe tot 38,2% (95% BI 34,8-41,6) en daalde daarna tot 8,5% (95% BI 6,5-11,1) in 2010 (trend test P<0,001), overeenkomstig met de afname in injecterend druggebruik. De prevalentie van onbeschermde seks in 1991 nam af van 55,6% (95%BI 42,3-48,5) tot 45,4% (95% BI 42,3-48,5) in 1996. Tussen 1997 en 2005 bleef dit relatief stabiel, maar daalde na 2005 tot 35,0% (95% BI 31,4-38,8) (trend test P<0,001). De prevalentie van zelfgerapporteerde soa was in 1986 6,3% (95% BI 4,3-9,2) en daalde tot 3,1% (95% BI 2,6-4,6) in 2010 (trend test, P =0,011).
Gedurende de 25-jarige observatieperiode zou een afname in risicogedrag veroorzaakt kunnen worden doordat deelnemers met hoog risicogedrag deelname beëindigden of overleden zijn. In een sensitiviteitsanalyse hebben we deelnemers met een studiebezoek in 2010 vergeleken met de totale groep. De trends in deze geselecteerde groep van zelfgerapporteerde soa, onbeschermde seks en het lenen van naalden waren vergelijkbaar met de totale groep. Injecterend druggebruik was gemiddeld lager in de geselecteerde groep vergeleken met de totale groep, dit verschil werd vanaf 1997 kleiner. Het gebruik van spuitomruil was ook lager in de geselecteerde groep, maar volgde dezelfde afname over de tijd (gegevens niet getoond). Om een cohorteffect uit te sluiten hebben we 3 jaar na intrede van de ACS de followuptijd gecensureerd. Trends waren vergelijkbaar, alhoewel we geen afname observeerden in onbeschermde seks na 2005.
Figuur 2 Gemodelleerde trends in zelfgerapporteerd injecterend en seksueel risicogedrag als proportie van het aantal bezoeken per kalenderjaar onder druggebruikers van de Amsterdam Cohort Studies, 1986-2011. De schaduw en gearceerde gebieden zijn de 95% betrouwbaarheidsintervallen
Soa en onbeschermde seks bij recente bezoekers
Tussen november 2010 en juni 2011 bezochten 272 personen de ACS waarvan 197 (72,4%) hebben deelgenomen aan de soascreening. Weigeraars aan de soascreening hadden geen interesse (64%), waren recentelijk getest (17,3% ) of hadden geen tijd (9,3%). Geslacht, leeftijd en nationaliteit van de weigeraars was vergelijkbaar met de recente bezoekers die wel toestemden tot deelname. Van de 75 weigeraars waren er 9 (12,0%) hivgeïnfecteerd, vergeleken met 25 van de 197 (12,7%) deelnemers aan de soascreening. Van belang is dat 65,3% van de weigeraars niet seksueel actief was in de 6 maanden voor het cohortbezoek vergeleken met 45,7% van de deelnemers die toestemden in soascreening (χ²-toets, P = 0,003).
Van de 197 recente bezoekers die deelnamen aan de soascreening, waren 141 (71,6%) mannen en de meerderheid had de Nederlandse nationaliteit (84,2%). De mediane leeftijd was 49,4 jaar (IKB 43,2-53,0; zie tabel 1). Bij alle deelnemers werd bloed afgenomen en bij 181 (91,9%) van de deelnemers werd urine of een vaginale swab getest op soa. Van alle deelnemers werden er 190 (96,4%) getest bij het cohort, de overige 7 (3,6%) werden gescreend op de soapolikliniek van de GGD vanwege hun verhoogd risicoprofiel. Van de 197 deelnemers hadden er 22 (11,2%) uitslagen passend bij een eerder behandelde syfillisinfectie. Van deze 22 deelnemers waren er 16 (72,7%) vrouw. Geen van de 197 deelnemers werd gediagnosticeerd met een actieve of onbehandelde syfilis. Van de 181 deelnemers werden 3 deelnemers (1,7%, allen vrouw en hivnegatief) gediagnosticeerd met CT. Geen van de 181 deelnemers had NG.
Determinanten van onbeschermde seks bij recente bezoekers
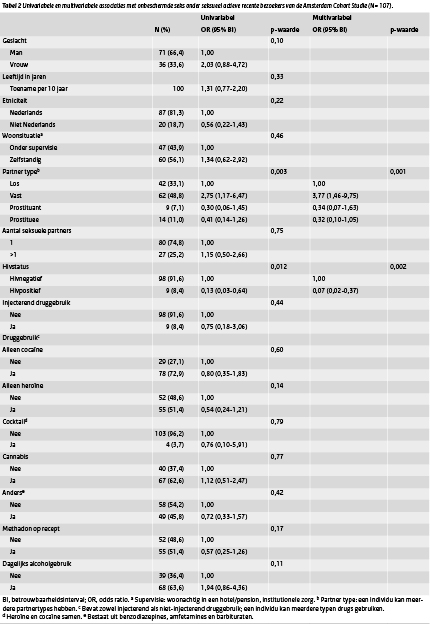
Vanwege de lage soaprevalentie bij de soascreening, maar de substantiële prevalentie onbeschermde seks in longitudinale analyses, werd besloten om determinanten van onbeschermde seks te analyseren. Van de 197 recente bezoekers rapporteerden 107 (54,3%) vaginale of anale seks in de afgelopen 6 maanden. Multivariabele analyse toonde aan dat het hebben van een vaste partner (aangepaste OR [aOR] 4,09; 95% BI 1,59-10,53) positief geassocieerd was met onbeschermde seks. Hivgeïnfecteerde deelnemers rapporteerden minder onbeschermde seks (aOR 0,07; 95% BI 0,02-0,37) vergeleken met hivnegatieve deelnemers (tabel 2).
Discussie
Deze studie beschrijft dalende trends in hivincidentie, injecterend druggebruik en seksueel risicogedrag onder druggebruikers van de ACS van 1986-2011. Daarnaast laat de soascreening onder deelnemers met een studiebezoek in de periode 2010-2011, een lage soaprevalentie zien. Hoewel onbeschermde seks vaak voorkomt is dit geassocieerd met seks met een vaste partner en komt onbeschermde seks minder vaak voor bij hivgeïnfecteerde deelnemers. Deze dalende trend in hivincidentie wordt ook gezien bij druggebruikers in andere Westerse landen. (2,12) Daarentegen is er in andere delen van de wereld sprake van een toename van de hivincidentie onder druggebruikers. (4,6,12) Deze epidemiologische discrepantie kan een resultaat zijn van ongelijke toegang tot harmreductionprogramma’s en hivbehandelcentra. (6)
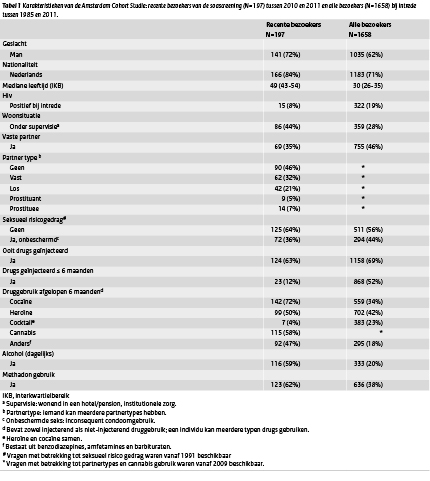
Tabel 1 Karakteristieken van de Amsterdam Cohort Studie: recente bezoekers van de soascreening (N=197) tussen 2010 en 2011 en alle bezoekers (N=1658) bij intrede tussen 1985 en 2011. Klik op de tabel voor een vergrote weergave in pdf
De toegankelijkheid van hivpreventie en behandel mogelijkheden is het hoogste in West-Europa waar 61% van de druggebruikers wordt bereikt. (13) In de jaren ‘80 startte Nederland als één van de eerste landen in West-Europa harmreductionprogramma’s. (6) Een studie die het effect onderzocht van spuitomruil en opiaatsubstitutietherapie op de incidentie van hiv en hepatitis C-virus (HCV (hepatitis C virus)) onder druggebruikers van de ACS, liet zien dat de combinatie van deze interventies geassocieerd was met een lager risico op het oplopen van hiv en HCV. (7) De gerapporteerde dalende trend van spuitomruil in deze studie wordt ook waargenomen in een afname van het absolute aantal uitgewisselde naalden per kalenderjaar in Amsterdam.
Naast het effect van harmreductionprogramma’s op het injecterend risicogedrag, lijkt injecterend druggebruik in Nederland uit de mode. In Amsterdam daalde het aantal jonge druggebruikers die ooit geïnjecteerd hadden van 88% in de periode 1985-1989, naar 31% in de periode 2000-2004. (14) Op Europees niveau injecteert minder dan 10% van alle beginnende druggebruikers. (12) Nederland heeft de laagste rate van beginnende injecterende druggebruikers van Europa, namelijk 2,1/100 PJ. (15) De veroudering van de populatie van de ACS en de drugpopulatie in zijn geheel is een andere mogelijke verklaring voor de dalende trends in risicogedrag. Druggebruikers ouder dan 50 jaar injecteren minder drugs en delen minder vaak naalden dan jongere gebruikers. (16) Daarnaast rapporteerden oudere druggebruikers minder seksuele contacten dan jongere druggebruikers. Echter, oudere druggebruikers die wel seks hebben, vertonen vaak verhoogd risicogedrag, zoals inconsequent condoomgebruik. (17) Uit de analyse onder recente bezoekers van de ACS kwam naar voren dat een groot aantal bezoekers geen seksuele partners rapporteerden in de afgelopen 6 maanden.
Tabel 2 Univariabele en multivariabele associaties met onbeschermde seks onder seksueel actieve recente bezoekers van de Amsterdam Cohort Studie (N= 107). Klik op tabel voor een vergrote weergave in pdf
De geobserveerde afname van risicogedrag zou verklaard kunnen worden door een selectief verlies van hoogrisicodeelnemers binnen het cohort. Om dit te onderzoeken hebben we een sensitiviteitsanalyse uitgevoerd waarbij we vergelijkbare dalingen constateerden tussen deelnemers met een bezoek in 2010 en de totale populatie druggebruikers van de ACS. Onze bevindingen zijn vergelijkbaar met surveillanceprogramma’s die laten zien dat diagnoses als nieuwe/acute hiv-, HBV (hepatitis B virus) (hepatitis B-virus)- en HCV-infecties zeldzaam zijn bij druggebruikers in Nederland. (18)
Uit een eerdere studie onder druggebruikers van de ACS tussen 1985 en 2005 bleek dat hiv-transmissie was verschoven van voornamelijk overdracht via naalden in de periode 1985 tot 1996, naar voornamelijk seksuele overdracht in de periode 1997 tot 2005. (8) Deze verandering is niet alleen in het belang van druggebruikers zelf, maar ook voor het risico op verspreiding naar andere groepen. Noemenswaardig is dat er geen toename is gevonden in seksueel risicogedrag onder hivgeïnfecteerde druggebruikers van de ACS die met antiretroviralecombinatietherapie zijn begonnen. (19) Daarnaast suggereren onze gegevens een voortzetting van de geleidelijke daling van onbeschermde seks vanaf 2004. Nog steeds is de prevalentie van onbeschermde seks onder druggebruikers substantieel, maar de analyse onder recente bezoekers laat zien dat onbeschermde seks met name plaatsvindt met een vaste partner en minder voorkomt bij hivgeïnfecteerde deelnemers. Dit wordt ondersteund door de lage soaprevalentie onder de recente bezoekers van de ACS (2,5%, uitsluitend CT). Gegevens van behandelcentra van druggebruikers en cohortstudies uit Groot-Brittannië en de Verenigde Staten lieten hogere prevalenties van CT en NG zien. (20,21) Een CT-screening onder jongeren (leeftijd 15-29 jaar) in Amsterdam in 2008 vond een prevalentie van 3,6%. (7) De dalende trends in seksueel risicogedrag en lage soaprevalentie wijzen erop dat het risico op seksuele transmissie van hiv onder druggebruikers laag is. Echter, de soascreening zou herhaald moeten worden om de lage soaprevalentie te bevestigen. Daarnaast zijn er meer gegevens nodig van soa bij druggebruikers buiten het cohort.
Deze studie heeft een aantal beperkingen. Ten eerste zijn onze resultaten niet generaliseerbaar naar jongere druggebruikers en naar degenen die in regio’s leven waar weinig of geen toegang is tot harmreductionprogramma’s. Ten tweede zijn de gegevens over druggebruik en seksueel risicogedrag zelf gerapporteerd. Dit kan leiden tot sociaal wenselijke antwoorden en een mogelijke onderschatting van het risicogedrag. De soascreening en de zelfgerapporteerde soa tonen echter vergelijkbare prevalenties. Ten derde is er gekozen voor zelfswabs om deelname aan de soascreening te verhogen. Hierdoor konden we niet op Trichomonas vaginalis (TV) screenen, terwijl andere studies hoge prevalenties van TV onder vrouwelijke druggebruikers rapporteerden. (20,21) Wij hadden alleen de mogelijkheid om TV te testen in de 7 hoogrisicodeelnemers die naar de soapoli werden verwezen.
Conclusie
Deze studie beschrijft dalende trends in hivincidentie, injecterend druggebruik en seksueel risicogedrag onder druggebruikers van de ACS van 1986-2011. Onbeschermde seks vindt met name plaats met een vaste partner en komt minder vaak voor onder hivgeïnfecteerde deelnemers. De dalende trends en de lage soaprevalentie bij recente bezoekers, wijzen op een geringe kans op hiv en soa. Deze bevindingen suggereren dat druggebruikers in Amsterdam geen significante rol meer spelen in de verspreiding van hiv.
De auteurs bedanken onderzoeksverpleegkundigen L.C del Grande en W.M van der Veldt voor de coördinatie, dataverzameling en bloedafnames; collega’s J. van der Helm en A. Matser voor statistische input; en alle deelnemers aan de studie.
Dit artikel is een bewerking van: Van der Knaap N, Grady BPX, Schim van der Loeff MF, Heijman T, Speksnijder A, et al. (2013) Drug Users in Amsterdam: Are They Still at Risk for HIV? PLoSONE 8(3): e59125. doi:10.1371/journal.pone.0059125
Auteurs
N. van der Knaap 1,2, B.P.X. Grady 1,3, M.F. Schim van der Loeff 1,3, T. Heijman 1,3, A. Speksnijder 1,4, R. Geskus 1,6, M. Prins 1,3,5
- GGD Amsterdam
- Universiteit van Amsterdam
- Center of Infectious diseases and Immunology Amsterdam (CINIMA), Academisch Medisch Centrum, Amsterdam
- Streeklaboratorium voor de Volksgezondheid en Bijzonder Instituut voor de Virologie, GGD Amsterdam
- Tropische Geneeskunde en AIDS, Academisch Medisch Centrum, Amsterdam
- Afdeling Klinische Epidemiologie, Biostatistiek en Bioinformatica, Academisch Medisch Centrum, Amsterdam
Correspondentie
bgrady@ggd.amsterdam.nl
- Booth RE, Kwiatkowski CF (Cystic Fibrosis), Chitwood DD. Sex related HIV (humaan immunodeficientievirus) risk behaviors: differential risks among injection drug users, crack smokers, and injection drug users who smoke crack. Drug Alcohol Depend. 2000;58(3):219-26.
- European Center for Disease Prevention and Control. HIV/AIDS surveillance in Europe 2010. 2011
- van Veen MG, Gotz HM, van Leeuwen PA, Prins M, van de Laar MJ. HIV and sexual risk behavior among commercial sex workers in the Netherlands. Arch Sex Behav. 2010;39(3):714-23.
- Strathdee SA, Stockman JK. Epidemiology of HIV among injecting and non-injecting drug users: current trends and implications for interventions. Curr HIV/AIDS Rep. 2010;7(2):99-106.
- Kuyper LM, Collins CL, Kerr T, et al. The prevalence and incidence of sexually transmitted infections in a prospective cohort of injection drug users in Vancouver, British Columbia. Can J Infect Dis Med Microbiol. 2005;16(4):225-9.
- Atun RA, McKee M, Coker R, Gurol-Urganci I. Health systems’ responses to 25 years of HIV in Europe: inequities persist and challenges remain. Health Policy. 2008;86(2-3):181-94.
- van Bergen JE, Fennema JS (Joint Strike Fighter), van den Broek IV (Informatievoorziening), Brouwers EE, de Feijter EM, Hoebe CJ, Koekenbier RH, de Coul EL, van Ravesteijn SM, Götz HM. Rationale, design, and results of the first screening round of a comprehensive, register-based, Chlamydia screening implementation programme in the Netherlands. http://www.ncbi.nlm.nih.gov/pubmed/20925966> BMC Infect Dis. 2010 Oct 7;10:293. doi: 10.1186/1471-2334-10-293. PMID: 20925966.
- Lindenburg CE (Conformité Européenne), Krol A, Smit C, et al. Decline in HIV incidence and injecting, but not in sexual risk behaviour, seen in drug users in Amsterdam: a 19-year prospective cohort study. AIDS. 2006;20(13):1771-5.
- de Vos AS, van der Helm JJ, Matser A, Prins M, Kretzschmar ME. Decline in incidence of HIV and hepatitis C virus infection among injecting drug users in Amsterdam; evidence for harm reduction? Addiction. 2013;108(6):1070-81.
- Hastie T, Tibshirani R. Generalized additive models for medical research. Stat Methods Med Res. 1995;4(3):187-96.
- Hanley JA, Negassa A, Edwardes MD, Forrester JE. Statistical analysis of correlated data using generalized estimating equations: an orientation. Am J Epidemiol. 2003;157(4):364-75.
- European Monitoring Centre for Drugs and Drug Addiction. Trends in injecting drug use in Europe. 2010
- Mathers BM, Degenhardt L, Ali H, et al. HIV prevention, treatment, and care services for people who inject drugs: a systematic review of global, regional, and national coverage. Lancet. 2010;375(9719):1014-28.
- van de Laar TJ, Langendam MW, Bruisten SM, et al. Changes in risk behavior and dynamics of hepatitis C virus infections among young drug users in Amsterdam, the Netherlands. J Med Virol. 2005;77(4):509-18.
- Buster MC (medisch centrum), Witteveen E, Prins M, et al. Transitions in drug use in a new generation of problem drug users in Amsterdam: a 6-year follow-up study. Eur Addict Res. 2009;15(4):179-87.
- Kwiatkowski CF, Booth RE. HIV risk behaviors among older American drug users. J Acquir Immune Defic Syndr. 2003;33 Suppl 2:S131-7.
- Savona N. Older people are at risk of sexually transmitted infections. Sex Transm Infect. 2011;87(1):70.
- Trienekens SCM, Koedijk FDH, van den Broek IVF, et al. National Institute for Public Health and the Environment. Sexually tranmsitted infections, including HIV, in the Netherlands. 2012
- Heijman TL, Van der Bij AK, De Vries HJ, Van Leent EJ, Thiesbrummel HF,et al. (2007). Effectiveness of a risk-based visitor-prioritizing system at a sexually transmitted infection outpatient clinic. Sex Transm Dis 34: 508–512.PMID: 17179775.
- Heymans R, Matser AA, Bruisten SM, Heijman T, Geskus RB (Robertson-Berger), et al. (2012). Distinct Neisseria gonorrhoeae transmission networks among men who have sex with men in Amsterdam, the Netherlands. J Infect Dis. PMID: 22693236.
- Plitt SS, Garfein RS (respiratoir syncytieel), Gaydos CA, et al. Prevalence and correlates of chlamydia trachomatis, neisseria gonorrhoeae, trichomonas vaginalis infections, and bacterial vaginosis among a cohort of young injection drug users in Baltimore, Maryland. Sex Transm Dis. 2005;32(7):446-53.