Infecties veroorzaakt door meticillineresistente Staphylococcus aureus (MRSA (Methicilline-resistente Staphylococcus aureus)) zijn moeilijk te behandelen door de ongevoeligheid van deze bacterie voor alle èta-lactam-antibiotica (zoals penicillines, cefalosporines en carbapenems) en hun wisselende gevoeligheid voor andere groepen antibiotica. Nederland heeft samen met Noorwegen en Zweden de laagste MRSA-prevalentie van Europa. In 2011 was 1,8% van de S. aureus-isolaten in Nederland een MRSA; dit is ten opzichte van 2010 een lichte stijging (1,6%). Surveillance is een belangrijk instrument om het effect van het MRSA-beleid te monitoren en te toetsen. Dit artikel beschrijft de bevindingen en bijzonderheden van de nationale surveillance van MRSA in 2011.
content
Auteur(s): A. Haenen, G.N. Pluister, M. van Luit, T. Bosch, M.E.O.C. Heck, S. de Greeff, A.J. de Neeling
Infectieziekten Bulletin, jaargang 23, nummer 7, september 2012
De medisch microbiologische laboratoria zenden sinds 1989 één MRSA (Methicilline-resistente Staphylococcus aureus)-isolaat van iedere positief bevonden patiënt of medewerker voor kosteloze typering naar het RIVM. Bovendien wordt de inzenders gevraagd een vragenlijst in te vullen voor ieder ingestuurd
isolaat (https://mrsa.rivm.nl/images/MRSA_vragenlijst2.doc). De ingevulde vragenlijst wordt per post of via de beveiligde webapplicatie OSIRIS (information system) naar het RIVM gestuurd.
De vragenlijst bevat naast beknopte epidemiologische gegevens ook vragen over mogelijke besmettingsroutes, en meer in het bijzonder tot welke WIP (Werkgroep Infectiepreventie) (Werkgroep Infectie Preventie)-categorie de MRSA-drager behoort. (3) De WIP onderscheidt op basis van het risico op MRSA-dragerschap een drietal categorieën: (I) bewezen MRSA-dragerschap, (II) hoog risico op dragerschap, (III) matig verhoogd risico op dragerschap.
Van alle ontvangen isolaten worden naast de genetische karakterisering een E-test uitgevoerd en een multiplex PCR (polymerase chain reaction) (Polymerase Chain Reaction) om de MRSA te confirmeren. De genetische karakterisering van de MRSA-isolaten gebeurt met Staphylococcus proteïne A-(spa-)typering. Bij spa-typering bepaalt men de DNA (deoxyribonucleic acid)-sequentie van de repeatregio in het spa-gen. (4) Informatie over het spa-type is terug te vinden op de website van de Ridom spa-server (http://www.spaserver.ridom.de). Op basis van het spa-type kan men een uitspraak doen over een eventuele epidemiologische link. De verspreiding van de verschillende MRSA spa-typen wordt in kaart gebracht op een interactieve website. De resultaten van de typeringen zijn voor de deelnemende laboratoria in te zien op de MRSA-website (http://www.rivm.nl/
mrsa). Het aantal unieke MRSA’s (één per patiënt of medewerker) die het RIVM heeft getypeerd staan op het publieke deel van deze website.
Resultaten
Voorkomen van MRSA-microbiologische analyse
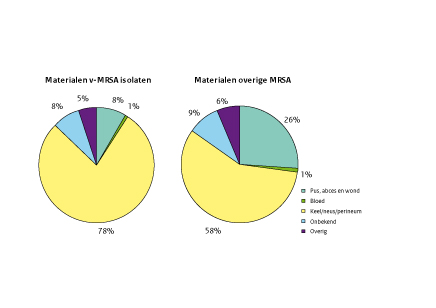
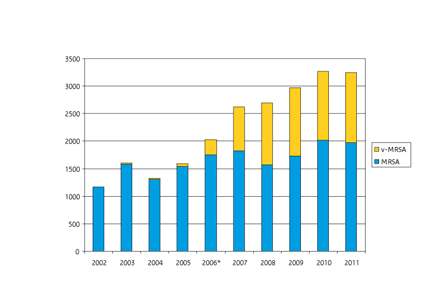
In 2011 hebben 65 laboratoria in totaal 3247 unieke MRSA-isolaten (1 isolaat per persoon) voor spa-typering ingestuurd naar het RIVM (figuur 2), 15 isolaten meer dan in 2010 (n=3232). (5) Het aantal veegerelateerde isolaten (v-MRSA), isolaten met een spa-type behorend tot het veegerelateerde CC398 (5), steeg met 27 isolaten van 38% in 2010 naar 39% in 2011. De materialen waaruit de isolaten in 2011 afkomstig waren zijn weergegeven in figuur 1. Op het aantal veegerelateerde bloedisolaten na, bleven de aantallen nagenoeg gelijk aan die van 2010. (Figuur 1) Het aantal veegerelateerde bloedisolaten is verdubbeld ten opzichte van 2010, maar deze stijging was niet significant.
Figuur 1 Aantal v-MRSA- en overige MRSA-isolaten per ingestuurd materiaal
Figuur 2 Aantal isolaten per jaar geïsoleerd tussen 2002 en 2011, en de proportie v-MRSA-isolaten. * In 2006 zijn de richtlijnen van de WIP aangepast en werd screening van varkens- en vleeskalverhouders ingevoerd.
Naast de mecA-bepaling wordt van alle ingestuurde isolaten ook de aanwezigheid van de PVL (Panton-Valentine leukocidine)-genen routinematig getest. Het mecA gen codeert voor de productie van een gemodificeerd penicillinebindend eiwit, het PBP-2a, dat een verminderde affiniteit heeft
voor bèta-lactam- antibiotica. Dit resulteert in een ongevoeligheid voor alle bèta-lactam- antibiotica. De PVL-genen coderen voor een toxine, het Panton-Valentine Leucocidine. Dit toxine kan leiden tot een hogere virulentie. PVL-genen werden bij 16% (n=535) van de isolaten gedetecteerd, dit is een stijging van 1% ten opzichte van 2010 en een stijging van 4% in vergelijking met 2009. Spa-type t008 was net als in 2010 het meest voorkomende PVL-positieve spa-type. Van de 260 spa-type t008 isolaten was 73% PVL+ (n=190), in 2010 was dit 63%, een significant verschil (p=0,013). Van de PVL-positieve isolaten was 42% (n=225) afkomstig uit keel- neus en perineumkweken. Van de PVL negatieve isolaten was dit 70,5% (n=1907). Van de PVL-positieve isolaten was 46% (n=244) afkomstig uit wonden en pus en 1% (n=4) uit bloed. Van de PVL-negatieve isolaten was 14% (n= 380) afkomstig uit wonden en pus en 1% (n=22) uit bloed.
De top 3 van meest gevonden spa-types is opgenomen in tabel 1.
|
Spa-type |
|
|---|---|
|
t011 |
824 (25%) |
|
t008 |
260 (8%) |
|
t108 |
231 (7%) |
Epidemiologisch analyse
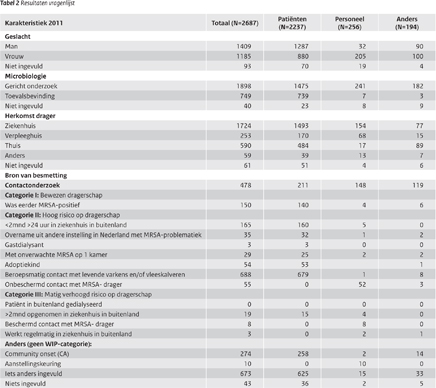
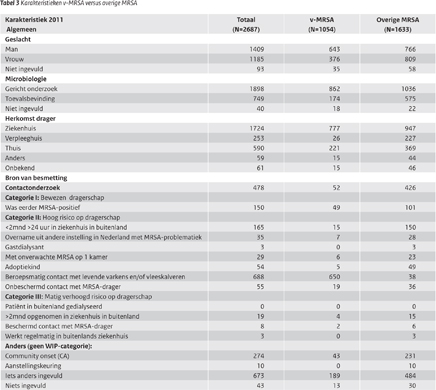
Met 83% (n=2687) van de isolaten werd ook een ingevulde vragenlijst meegestuurd. De resultaten van de vragenlijsten staan in tabel 2 en 3. De hierna besproken resultaten hebben, tenzij anders vermeld, betrekking op de 2687 isolaten waarvan een vragenlijst beschikbaar was. De resultaten worden per onderdeel van de vragenlijst weergegeven.
Vragenlijst deel A-Algemeen
Bijna driekwart van de MRSA-isolaten werd, net als in 2009 en 2010, gevonden met gericht onderzoek (n=1898), de overige MRSA werd bij toeval gevonden. Het merendeel van de MRSA-dragers verbleef op het moment van kweekafname in het ziekenhuis, 64% (n=1724). Een percentage van 22% (n=597) verbleef thuis. Daar werd bij de meeste personen de kweek afgenomen door de huisarts bij 4 personen gebeurde dit door een medewerker van een thuiszorginstelling, bij 3 door een verloskundige en bij 1 door een medewerker van een dialysecentrum. 9% (n=253) Van de dragers verbleef in een verpleeghuis; dit was een significante stijging van 5% (p=0,024) ten opzichte van 2010. De andere isolaten kwamen uit de groep van daklozen (n=6), uit verzorgingshuizen (n=2), asielzoekerscentra (n=3), een privékliniek (n=3), instellingen voor verstandelijke gehandicapten (n=2), revalidatiecentra (n=1) en een gevangenis (n=1). Van de overige isolaten (n=33) was de verblijfplaats van de drager onbekend.
Vragenlijst deel B-WIP-categorieën
Categorie I: Bewezen MRSA-dragerschap
Een percentage van 6% van de dragers (n=150) was, net als in 2010, bij opname of behandeling al bekend met MRSA.
Categorie II: Hoog risico op MRSA-dragerschap
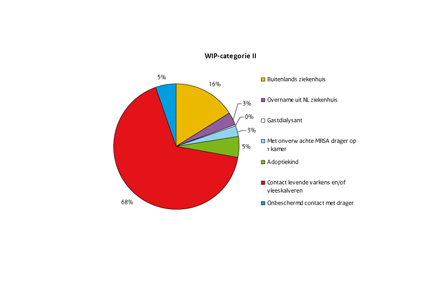
Van het totale aantal dragers viel 38% (n=1029) in categorie II, in categorie II vallen de volgende risicogroepen:
- Varkens- en vleeskalverhouders en andere personen die beroepsmatig contact hebben met levende varkens en of vleeskalveren;
- Personen die 2 maanden voorafgaand aan de opname of behandeling langer dan 24 uur in een buitenlands ziekenhuisopgenomen waren;
- Personen die zijn overgeplaatst uit een instelling waar een MRSA-epidemie heerste die niet onder controle was.
- Personen met onbeschermd contact met een MRSA-drager;
- Adoptiekinderen;
- Personen die met een onverwachte MRSA-drager op éénkamer lagen;
- Het meest voorkomende land van herkomst van adoptiekinderen was China (n=36).
Figuur 3 Aandeel per risicogroep in categorie II
Klik op onderstaande tabellen voor een grote pdf-versie hiervan.
Categorie III: Matig verhoogd risico op MRSA-dragerschap
In totaal viel 1% (n=30) van de MRSA-dragers in categorie III; 63% (n=19) daarvan waren personen die langer dan 2 maanden voorafgaand aan de opname of behandeling in Nederland in een buitenlands ziekenhuis waren opgenomen. Een kwart van de personen had beschermd contact gehad met een MRSA-drager, de helft daarvan (n=4) waren medewerkers van een verpleeghuis de andere waren medewerkers uit een ziekenhuis. Slechts 10% (n=3) werkte regelmatig in een buitenlands ziekenhuis.
Anders (geen WIP-categorie)
Van alle 2687 MRSA-dragers met een ingevulde vragenlijst viel in 2011 37% (n=1000) niet in een WIP-categorie. Bij 10% (n=274) van de MRSA-dragers was community onset aangegeven. Op 2% (n=43) van de vragenlijsten was niets aangegeven over de mogelijke oorzaak van het MRSA-dragerschap. Het percentage vragenlijsten waar een mogelijke andere bron van MRSA werd genoemd, bedroeg 25% (n=673 Er werd genoemd: een positief familielid 12% (n=81), personen die uit het buitenland kwamen of daar gereisd hadden 6% (n=43), contact met vee anders dan omschreven in de WIP 4% (n=26). In kleinere aantallen werden genoemd: afkomstig uit een verpleeghuis zonder een bekend MRSA-probleem 2% (n=13), zeemannen 2% (n=13), afkomstig uit een ziekenhuis zonder MRSA-probleem 1% (n=6), personen met onderliggend lijden 1% (n=6), afkomstig uit een verzorgingshuis zonder bekend MRSA-probleem 0,5% (n=4) en verzorgd door de thuiszorg 0,5% (n=2). Bij het grootste deel was de bron onbekend, 73% (n=455).
Het percentage personen dat werd gevonden bij een contactonderzoek was 18% (n=478).
Veegerelateerde MRSA
Bij 83% (n=1054) van de veegerelateerde isolaten was een ingevulde vragenlijst meegestuurd. In tabel 3 staan de karakteristieken van de veegerelateerde MRSA (v-MRSA) versus de niet-veegerelateerde MRSA (overige MRSA). Bij de v-MRSA was 36% vrouw en61% man en bij de overige MRSA was dat 52% versus 44%. MRSA bij toeval gevonden in een kweek kwam vaker voor bij personen met overige MRSA 35% (n=575) dan bij personen met v-MRSA 17% (n=174). Zowel kweken van v-MRSA-dragers als van overige MRSA-dragers kwamen voor het grootste deel uit een ziekenhuis, respectievelijk 74% (n=777) en 58% (n=947). Bij slechts 2 % (n=26) van de v-MRSA-dragers was een kweek afgenomen in een verpleeghuis, binnen de overige MRSA-dragers was dat percentage 14% (n=227). Het grootste deel van de v-MRSA-dragers had contact met levende varkens en/of vleeskalveren, 62% (n=650). Bij 38% (n=404) was er een andere bron van MRSA. 5% (n=49) Was al eens eerder positief voor MRSA getest en viel daarmee in WIP- categorie I. Vijftien personen waren korter dan 2 maanden geleden langer dan 24 uur in een buitenlandsziekenhuis opgenomen (1%). Negentien personen hadden onbeschermd contact gehad met een MRSA-drager (2%). Bij 4% (n=43) van de v-MRSA-dragers werd community onset vermeld. Bij 18% (n=189) werd een andere mogelijke reden voor MRSA-dragerschap aangegeven. Bij 27 personen was er wel veecontact. Dat contact was echter op een andere wijze of met andere dieren dan in de WIP beschreven. Twee personen hielden kippen, 2 waren slager, 2 waren voorheen varkenshouder, 1 persoon had een nertsenfokkerij, 1 had een veevoederbedrijf en 1 was de echtgenote van een dierenarts. De rest (n=18) woonde op een veehouderij of kwam daar geregeld maar gaf aan geen contact met de dieren te hebben. Elf mensen hadden een familielid dat v-MRSA-positief was en 1 v-MRSA-drager was in het buitenland geweest maar was daar niet in een ziekenhuis opgenomen.
Vragenlijst deel B-Contactonderzoek
In totaal waren er 268 contactonderzoeken waar 478 personen bij betrokken waren. (Tabel 3) Bijna 46% (n=124) resulteerde in een bron met een besmet contact terwijl van 31% (n=83) de bron niet aangegeven was. In de overige contactonderzoeken (23%, n=61) werden naast de bron 2 of meer positieve contacten gevonden met als maximum 16 positieve contacten. Bij 57% (n=35) daarvan werd hetzelfde spa-type gevonden als bij de bron. Bij 43% (n=26) was
het gevonden spa-type bij de bron anders dan van het contact c.q. de contacten.
In totaal werden 52 personen met een v-MRSA gevonden bij 45 contactonderzoeken. (Tabel 3) Bij 55% (n=25) van deze v-MRSAcontactonderzoeken was er 1 bron met 1 besmet contact. Bij 15% (n=7) van de v-MRSA-contactonderzoeken was er 1 bron en 2 positieve contacten en bij 30% (n=13) is de bron niet aangegeven. In 6 van de contactonderzoeken was sprake van een ander spa-type dan de indexpatiënt en was het spa-type van de contact(en) niet veegerelateerd.
Discussie
In 2011 is het aantal ingestuurde unieke isolaten vrijwel gelijk gebleven ten opzichte van 2010. In 2010 stabiliseerde het percentage v-MRSA al, in 2011 bleef het percentage vrijwel gelijk, 39% ten opzichte van 38% in 2010. Verder is het percentage personen wat al bekend MRSA-positief was bij opname met 6% gelijk gebleven aan 2010 terwijl dit percentage in 2009 nog 3,5% was. Binnen de groep v-MRSA-dragers steeg dit percentage van 2% in 2009 naar 4% in 2010 naar 5% in 2011. Het werkelijke percentage bekende dragers was waarschijnlijk hoger want maar 1 isolaat per drager wordt kosteloos getypeerd, tenzij het tweede isolaat langer dan 1 jaar na het eerste is afgenomen. Het percentage personen met MRSA dat uit een buitenlands ziekenhuis kwam, was in 2011 gelijk aan het percentage in 2010
(6%). In 2008 en 2009 was dat percentage 8%. Als de veegerelateerde isolaten, vanwege het noemereffect, buiten beschouwing worden gelaten, bleef het percentage in 2011 (9%) ook nagenoeg gelijk aan het percentage in 2010 (8%). In 2010 is de laboratoria gevraagd om voor de typering niet een screeningsisolaat van de betreffende persoon in te sturen maar, indien voorhanden, het isolaat van een infectie. In 2011 was 20% van de isolaten een zogenaamd infectie-isolaat (verkregen uit bloed, pus, abces of wond), gelijk aan 2009 en 2010. De vraag om infectie-isolaten in te sturen heeft dus geen invloed gehad op het percentage ingestuurde isolaten. Het aantal isolaten afkomstig van personen uit verpleeghuizen is in 2011 met 1,5% significant gestegen ten opzichte van 2010.\
Het aantal ingestuurde isolaten van personen die op moment van kweekafname in een ziekenhuis en thuis verbleven is met 2% gedaald ten opzicht van 2010. Op 13 vragenlijsten was aangegeven dat de MRSA-drager niet in 1 van de WIP-categorieën thuis hoorde, maar wel fkomstig was uit een verpleeghuis waarbinnen geen sprake was van een bekend MRSA-probleem. Greenland et al. meldden een MRSA- prevalentie van 0.33% in 2011 in de verpleeghuizen (6). In de nationale surveillance is de noemer, het totale aantal personen waarbij kweekonderzoek is gedaan, met betrekking tot verpleeghuizen niet voorhanden. Het is dus niet te zeggen of er een indicatie is dat de MRSA-problematiek in de verpleeghuizen toeneemt of dat er meer diagnostiek wordt verricht.
In 2011 werden 271 contactonderzoeken gemeld, een stijging van 3% ten opzichte van 2010. Bij 43% bleken de spa-typen van de index en de contacten niet met elkaar overeen te komen,wat wil zeggen dat de in de praktijk veronderstelde bron niet voor verspreiding heeft gezorgd. Deze onverwachte bevindingen zijn niet goed te verklaren.
Ruim eenderde (n=1000) van alle MRSA-dragers behoorde niet tot de bekende risicocategorieën van de WIP. Bij 67% daarvan is iets anders ingevuld. Daarvan was bij 73% de bron onbekend, vorig jaar was dat percentage 75%.
Tot besluit
De WIP heeft onlangs de MRSA-richtlijn herzien. Een van de wijzigingen in deze herziene richtlijn is dat huisgenoten, seksuele partners en verzorgenden die onbeschermd contact hebben met MRSA-positieve personen tot risicocategorie 2 worden gerekend. In de Nederlandse surveillance is te zien dat 12% van de MRSAdragers contact hadden met een MRSA-positieve huisgenoot of familielid. Een tweede wijziging in de richtlijn is dat medewerkers die beschermd contact hebben gehad niet meer vallen onder risicocategorie 3, omdat het risico op transmissie zeer klein is voor deze medewerkers. In de surveillancedata is te zien dat bij 3% van de vragenlijsten ingevuld is dat een medewerker MRSA-positief is geworden na beschermd contact met een MRSA-drager. De surveillance data geven echter geen informatie hoeveel personen beschermd contact hebben gehad en hoeveel daarvan geen MRSA-drager zijn geworden.
Met ingang van februari 2012 wordt ook het MLVA (Multi-Locus Variable number of tandem repeat Analysis)-type (Multiple- Locus variable number tandem repeat analysis) gerapporteerd aan de inzenders van isolaten/kweken. (7) De resultaten daarvan zijn ook te vinden op de website (http://www.rivm.mrsa.nl). De MLVA-typering kan naast de spa-typering gebruikt worden om transmissieroutes en bronnen te identificeren.
Auteurs
A. Haenen, G.N. Pluister, M. van Luit, T. Bosch, M.E.O.C. Heck, S. de Greeff, A.J. de Neeling, Centrum Infectieziektebestrijding, RIVM,
Bilthoven en alle participerende laboratoria
Correspondentie | A. Haenen | Anja.Haenen@rivm.nl
Literatuur
- Antimicrobial resistance surveillance in Europe 2009. Annual report of the European Antimicrobial Resistance Surveillance Network (EARS (European Antimicrobial Resistance Surveillance System)-net): www.earss.rivm.nl.
- Stichting Werkgroep Antibioticabeleid (SWAB). NethMap (Consumption of antimicrobial agents and antimicrobial resistance among medically important bacteria in the Netherlands) 2011 – Consumption of antimicrobial agents and antimicrobial resistance among medically important bacteria in the Netherlands: www.swab.
- MRSA-richtlijn Werkgroep Infectie Preventie (WIP): www.wip.nl.
- Harmsen D., H. Claus, et al. Typing of methicillin-resistantStaphylococcus aureus in a university hospital setting by using novel software for spa repeat determination and database management. J Clin Microbiol 2003; 41(12): 5442-8.
- Haenen A. et al. Surveillance van MRSA in Nederland in 2010. Infectieziekten Bulletin 2011; 22 (B): 6-11.
- Greenland K. et al. Low prevalence of Methicillin-resistant Staphylococcus aureus in Dutch nursing homes. Journal of the American Geriatrics Society April 2011; 59 (4):768-769
- Schouls L. et al. Multiple-Locus Variable Number Tandem Repeat Analysis of Staphylococcus Aureus: Comparison with Pulsed-Filed Gel Electrophoresis and spa-typing. PLoS (Plos One) ONE 2009; 4 (4): e5082